표준 상태, 표준 엔탈피, 표준 자유에너지
Standard state, Standard enthalpy, Standard free energy
0. 들어가기
표준 반응 자유 에너지(ΔrG ˚)와 반응 자유에너지(ΔrG )의 관계를 오인하는 경우가 종종 있다. 이전 글(151)에서도 관련 내용을 짧게 언급했었다.
가장 대표적이면서도 쉽게 빠지는 오류가 ΔrG ˚(표준 반응 자유에너지)와 ΔrG (반응 자유에너지)를 25 ℃의 자유에너지와 그 외 온도의 자유에너지로 구분하는 것이다.
사실, 이렇게 구분하면 ΔG ˚ = ΔH ˚ - TΔS ˚ 식의 온도항에 25 ℃(298.15 K) 외의 값이 대입되는 상황을 이해할 수가 없어진다. 왜냐하면, ΔG ˚가 오직 25 ℃에서의 자유에너지만을 나타내는 것이라고 생각하고 있기 때문이다.
* 잘못된 구분 *
- 표준 반응 자유에너지(ΔrG ˚) : 25 ℃ 온도 조건에서 진행된 반응의 자유에너지 변화량
- 반응 자유에너지(ΔrG ) : 그 외 온도 조건에서 진행된 반응의 자유에너지 변화량
* 올바른 구분 *
- 표준 반응 자유에너지(ΔrG ˚) : 지정 온도, 표준 상태 반응물과 표준 상태 생성물의 자유에너지 차이
- 반응 자유에너지(ΔrG ) : 반응 진행에 따른 반응계(반응물+생성물)의 총 자유에너지 변화량(기울기)
위와 같은 문제가 왜 발생한 걸까에 대해 생각해보았다. 지극히 단순한 추측이지만, 크게 두 가지 정도가 마음에 걸렸다.
원인은 '명확치 않은 표준 상태의 정의'와 열화학 단원에서 자주 접하는'25 ℃ 기준의 표준 열역학적 데이터'이다.
* 문제 상황 재연 *
1) 먼저, 표준 상태의 정의를 '25 ℃, 1 기압' 정도의 조건으로 생각하고 간단히 넘긴다.
2) 열화학 단원을 학습하면서 표준 열역학적 데이터를 처음 접한다.
3) 표의 데이터가 25 ℃ 기준으로 측정 또는 계산되었다는 사실과 '표준' 열역학적 데이터라는 이름이 함께 눈에 들어온다.
4) 이를 이용한 다수의 문제를 해결하면서 개념을 학습한다.
5) 자연스럽게 '표준'이라는 용어와 '25 ℃의 온도'가 연결되고, 표준 = 25 ℃의 의미로 받아들인다.
- 과거의 내가 잘못된 구분을 했던 이유분석변명 -
사실, 과거의 나 역시 많이 헷갈렸고, 모호했던 부분이다. 이로 인해 수업 중에 잘못된 정보를 전달한 적도 있다.(미안! 얘들아! 그래도 잘 컸..?)
그런데 최근 동료 선생님께서 이와 관련된 비슷한 질문을 하시고, 인터넷 상에도 관련 질문 글들이 심심찮게 보여서 이와 관련된 이야기를 한 번쯤은 정리해놔야겠다는 생각을 하게 되었다.
이후 하나씩 언급하겠지만 '표준(standard)'을 정의할 때, 온도는 특정되지 않는다. 표준이라는 용어와 25 ℃를 되도록 멀리 떨어뜨려, 별개의 것으로 생각하게 하는 것이 이번 글의 주된 목적이다. (그런데, 끝까지 읽기 쉽지 않을 듯 하다. 목적 달성은 쉽지 않을 것 같다.)
1. 표준 상태 (standard state)
'표준 상태'는 특정 조건에 놓인 물질의 '상태'를 나타내는 표현이다. 물질이 놓인 '조건'(condition)이 아니라 '상태'(state)를 말한다.
반면, 아보가드로 법칙을 배울 때, 함께 등장하는 표준 온도와 압력(STP)은 물질이 놓인 '조건'이다. 일종의 표준화된 조건(standard condition, 273.15 K, 1 bar)이다.
- STP(273.15 K, 1 bar) '조건'에서 모든 기체 1 몰의 부피는 22.4 L로 동일하다.
- 298.15 K에서 탄소의 표준 '상태'는 흑연(graphite)이다.
물질은 온도와 압력, 그 밖의 조건에 따라 다양한 상태를 갖는다. 물질 입자 간 거리에 따라 고체, 액체, 기체로 구분되고, 원소는 여러 동소체를 갖기도 한다. '표준 상태'는 이러한 물질의 여러 상태 중 기준이 되는 하나의 상태를 나타낸다.
그렇다면, 물질의 여러 상태 중 어느 것이, 또 어떤 기준에 의해 표준 상태로 정해질까? 국제순수응용화학연합(IUPAC)에서는 표준 상태를 다음과 같이 정의한다.
지정 온도, 1 bar (=105 Pa) 압력 조건에서 열역학적으로 가장 안정한 물질의 상태
* 참고로, 1982 년 이전까지는 표준 압력(P ˚)이 1 기압(=1.01325 bar)이었으나 1982 년부터 1 bar(=0.986923 기압)로 변경되었다.
* 대부분의 화학책이 1982 년 이전부터 쓰였고, 고등학교 화학, 대학교 일반화학 수준에서는 압력 단위로 'bar'를 자주 사용하지 않아 여전히 '1 기압' 이라는 표현이 익숙할 수 있다. 본 글에서는 표준 압력 기준을 명확히 하고자 구태여 'bar' 를 사용했다.
표준 상태 정의 중, 눈에 띄는 점은 구체적인 온도 기준이 없다는 것이다. 세부 정의를 통해 조금 더 살펴보자.
1) 원소의 표준 상태는 1 bar, 지정 온도에서 동소체 중 가장 안정한 원소 상태로 정의한다.
2) 고체와 액체 물질의 표준 상태는 1 bar, 지정 온도에서 가장 안정한 상태로 정의한다.
3) 기체의 표준 상태는 1 bar 압력, 지정 온도에서 이상 기체 거동을 하는 기체 상태로 정의한다.
4) 용액 내 용해된 화학종의 표준 상태는 1 bar, 지정 온도에서 이상 용액처럼 행동하는 1 M 용액 상태로 정의한다.
1) ~ 4) 모두, 압력은 1 bar로 분명하게 표현된 것에 비해, 온도는 그냥 '지정 온도'다. 이는 어떤 온도를 지정했느냐에 따라 물질의 표준 상태가 다를 수 있다는 말이다. H2O 를 예로 들어보자.

248.15 K(-25 ℃), 1 bar에서 H2O 표준 상태는 H2O (s ), 얼음이다. 반면, 298.15 K(25 ℃), 1 bar에서 H2O 표준 상태는 H2O (l ), 물이다. IUPAC 정의에 따라 지정 온도에서 열역학적으로 가장 안정한 H2O 상태가 얼음과 물이기 때문이다.
혹시라도, 온도가 따로 지정되지 않은 경우에는 298.15 K(25 ℃)로 생각하는 것이 일반적이다. 이유는 앞으로 다룰 표준 물리량(엔탈피, 자유 에너지)과도 관련이 있다.
2. 표준 엔탈피 (ΔH ˚)와 표준 자유에너지 (ΔG ˚)
가. 표준 반응 엔탈피와 자유에너지
엔탈피(H )나 자유에너지(G )와 같은 물리량은 물질의 에너지와 관련있다. 엔탈피와 자유에너지의 절대적인 값은 내부 에너지(U )와 마찬가지로 측정하거나 계산될 수 없다. [참고] 계와 내부 에너지(233)
하지만 다행스럽게도 화학자들은 물질 자체보다 변화에 관심 있다. 따라서 물질 고유 에너지 값보다는 반응에서의 에너지 변화량에 주목한다.
예를 들어 물질 A → B 반응이 있을 때, A, B 각각의 고유 에너지에는 관심이 없지만 A → B 과정에서 발생하는 반응열에는 관심을 갖는다. A에서 B로 변할 때, 열량계로 반응열을 측정하면 반응 전후의 엔탈피 변화량(반응 엔탈피, ΔH )를 알 수 있다.
A → B ΔH = HB - HA
다만, 압력, 온도, 물질의 상태, 물질의 양 등이 달라지면, 물질의 고유 에너지 값이 달라지며, 이는 반응에서의 에너지 변화에도 영향을 준다. 따라서 반응이 진행되는 조건이 고정되고, 분명할수록 좋다. 반응 전후 에너지 변화를 폭넓게 다루기 위해서는 반응에 대한 보편적 기준이 필요하다.
이에 지정된 온도 조건에서 '표준 상태 반응물'이 '표준 상태 생성물'로 변할 때를 '표준 반응'으로 기준 삼았다. 그리고, 이 과정에서의 에너지 변화를 표준 반응 엔탈피(ΔH ˚)와 표준 반응 자유에너지(ΔG ˚)로 정했다.
* 표준 반응에서의 에너지 변화
- 표준 반응 엔탈피(ΔrH ˚) : 지정 온도, '표준 상태 반응물'과 '표준 상태 생성물'의 엔탈피의 단순 차이
- 표준 반응 자유에너지(ΔrG ˚) : 지정 온도, '표준 상태 반응물'과 '표준 상태 생성물'의 자유에너지의 단순 차이
표준 반응을 만족하기 위해서는 반응물과 생성물이 모두 '표준 상태'여야 한다. 표준 상태 물질은 모두 순수한(pure) 상태여야 하므로, 반응물과 생성물이 공존하는 평형 상태를 갖거나 다른 부반응이 일어나면 안 된다. 반드시 완결되어야 하며, 반응 전후 지정 온도, 1 bar 조건 역시 유지되어야 한다.
* 참고로, 물리량의 표준 상태를 나타낼 때 위첨자로 ˚(노트, "naught")를 붙인다. 예를 들어 298.15 K에서의 표준 상태 엔탈피 변화(표준 반응 엔탈피)와 373.15 K에서의 표준 상태 자유에너지 변화(표준 반응 자유에너지)는 다음과 같이 표현한다.
ΔH ˚298.15 K , ΔG ˚373.15 K (지정 온도, 1 bar)
* 물리량의 표준 상태는 지정한 온도에 따라 다를 수 있기 때문에 위와 같이 온도를 아래 첨자로 따로 표현해주는 것이 좋다. 물리량 기호에 함께 표현한 ˚(naught)는 표준 상태라는 의미만을 가질 뿐이다. (물론, 온도가 생략되었다면 보통은 298.15 K으로 취급한다.)
나. 표준 생성 엔탈피와 자유에너지
표준 상태의 반응물이 표준 상태의 생성물로 변하는 반응을 기준으로 설정했으나 이것만으로 화학에서의 다양한 반응을 설명하기에는 상당히 제한적이다. 흑연(Cgraphite (s))과 산소 기체(O2 (g))가 만나 이산화탄소 기체(CO2 (g))를 생성하는 등의 몇몇 반응만을 말하기 때문이다.
Cgraphite (s ) + O2 (g ) → CO2 (g ) (지정 온도, 1 bar)
화학자들은 표준 반응 엔탈피(ΔH ˚)와 자유에너지(ΔG ˚)의 기준에 관한 한 가지 사항에 합의하였다.
"298.15 K, 표준 상태 원소(홑원소 물질)의 엔탈피(H )와 자유에너지(G ) 값은 0 [kJ/mol]이다." 1
위 문장을 세부적으로 살펴보면,
먼저, 온도가 298.15 K로 고정되었다. 또한 표준 상태의 원소에만 국한되는 사항이다. 즉, 298.15 K 조건에서, 반응에 관여하는 반응물 또는 생성물 중 '표준 상태의 원소'의 고유 에너지(엔탈피, 자유에너지) 값을 모두 0 [kJ/mol]으로 기준하자는 약속이다.
여기서의 온도 298.15 K와 표준 상태의 원소라는 조건은 열역학적 물리량(엔탈피, 자유 에너지)의 기준점이 되어주는 일종의 '열역학적 표준 조건(standard condition)'이라 할 수 있다.
앞서 제시한 흑연과 산소 기체를 통한 이산화탄소 기체의 생성 반응을 298.15 K, 1 bar 표준 조건에서 진행시키고 표준 반응 엔탈피(ΔH ˚298.15 K)를 측정한면,
해당 조건에서 반응물인 흑연과 산소 기체의 엔탈피는 모두 0 [kJ/mol] 이므로 표준 반응 엔탈피(ΔH ˚298.15 K) = -393.51 [kJ/mol]은 곧, 이산화탄소의 표준 생성 엔탈피(ΔfH ˚CO2)가 된다.
Cgraphite (s ) + O2 (g ) → CO2 (g ) ΔH ˚298.15 K = ΔfH ˚CO2 = - 393.51 [kJ/mol]
* 표준 생성 엔탈피의 아래 첨자 f는 생성을 뜻하는 formation에서 왔다.
즉, 열역학적 표준 조건(298.15K, 표준 상태)에서 '원소'의 엔탈피(그리고 자유 에너지)가 0 [kJ/mol]이라는 약속을 바탕으로 표준 상태 '화합물'의 표준 생성 엔탈피를 구할 수 있게 된 것이다.
3. 298.15 K에서 표준 상태가 아닌 물질의 표준 생성 엔탈피?
298.15 K 조건에서 표준 상태인 물질의 생성 엔탈피(그리고 자유에너지)만을 알 수 있는 것은 아니다. 대부분의 화학책 뒷부분에 첨부된 열역학적 데이터를 보면, 해당 조건에서 표준 상태가 아님에도 표준 생성 엔탈피(ΔfH ˚)와 자유에너지(ΔfG ˚) 값이 나와있음을 확인할 수 있다.

이는 엔탈피와 자유에너지가 모두, 반응 경로와는 무관한 상태 함수(state function)이기 때문에 가능한 일이다. 헤스의 법칙(Hess' Law)을 통해 적절한 다른 반응들을 몇차례 거쳐서 계산된 또는 측정된 값 들이다.
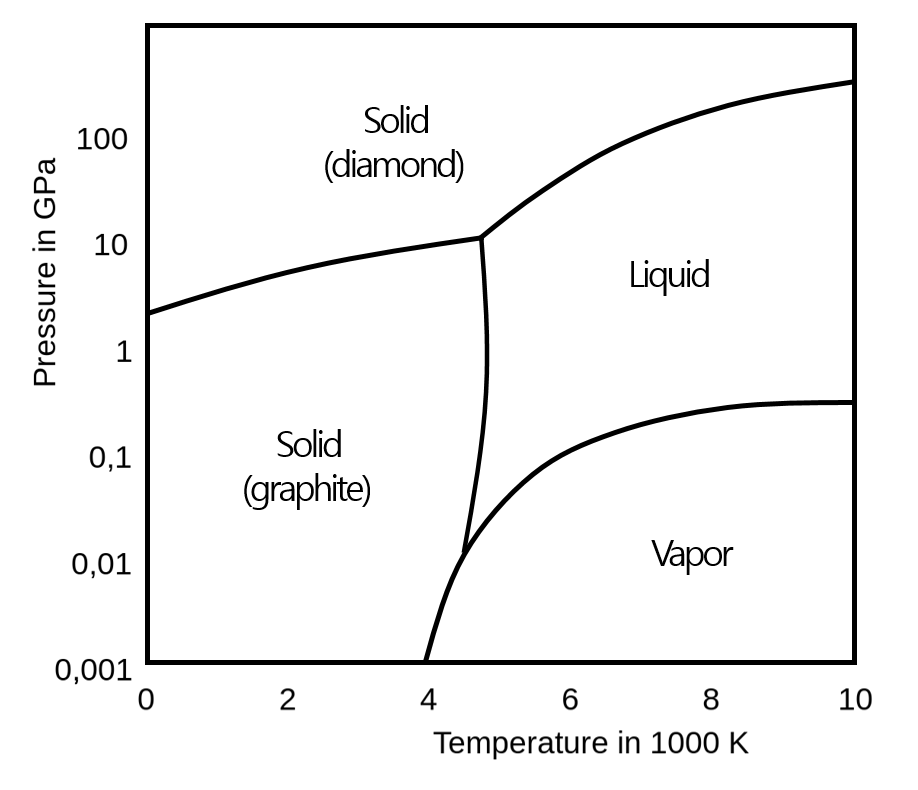
일례로 298.15 K, 1 bar(=0.0001 GPa)에서 탄소의 표준 상태는 흑연(graphite)이며, 다이아몬드는 열역학적으로 가장 안정한 상태가 아니므로 표준 상태가 아니다. 하지만, 해당 온도와 압력 조건에서의 연소 반응과 헤스의 법칙 등을 통해, 다음과 같이 다이아몬드의 표준 생성 엔탈피(ΔfH ˚298.15 K(dia))를 구할 수 있다.
(1) Cgraphite (s) + O2 (g) → CO2 (g) Δ연소H ˚298.15 K(gr) = - 393.51 [kJ/mol]
(2) Cdiamond (s) + O2 (g) → CO2 (g) Δ연소H ˚298.15 K(dia) = - 395.405 [kJ/mol]
(1) - (2)
Cgraphite (s) → Cdiamond (s) ΔH ˚298.15 K(gr) - ΔH ˚298.15 K(dia) = - 393.51 + 395.405 = +1.895 [kJ/mol]
표준 상태, 표준 엔탈피, 표준 자유에너지
-끝-
* 끝까지 읽어주셔서 감사합니다. 관련 내용에 대한 궁금증이나 오류 등에 대해 코멘트 주시면, 빠른 시일 내에 정정 혹은 답변드리도록 하겠습니다.
* 본문에 사용된 화학 용어 [출처] IUPAC Compendium of Chemical Terminolog Gold Book
1) 표준 상태 (standard state)

2) 표준 압력 (standard pressure, P ˚)
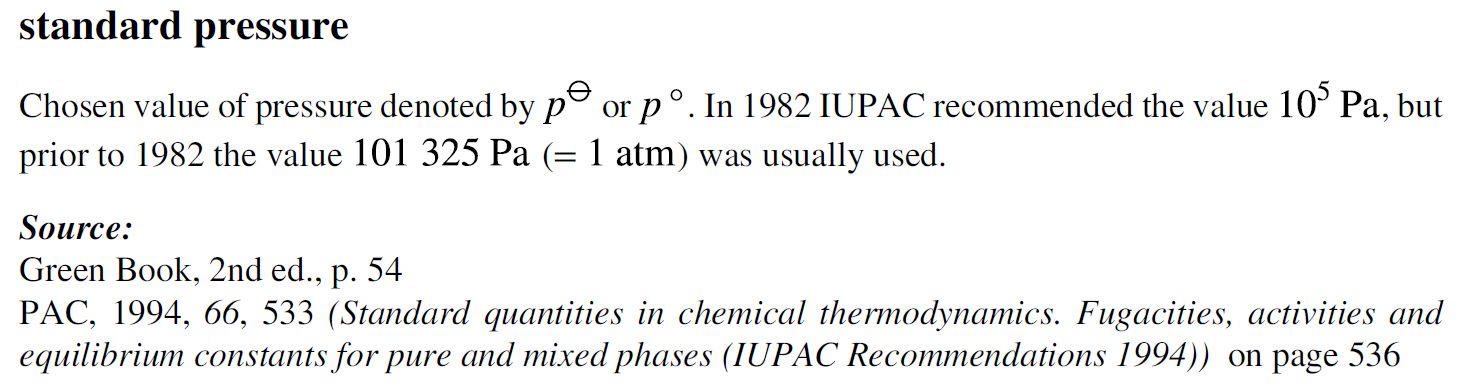
3) 기체에 대한 표준 압력 및 온도 조건 (standard conditions for gases, STP)

4) 표준 반응 (물리)량 (standard reaction quantities)

5) 열역학적 표준 물리량 (standard thermodynamic quantities)

- 정확하게는 298 K, 표준상태 가장 안정한 원소의 생성 반응(formation reaction, 원소 A → 원소 A)의 엔탈피와 자유에너지 변화량을 0 [kJ/mol]로 정하였다. [본문으로]
'화학 > 화학이야기' 카테고리의 다른 글
| 원자가 결합 이론 (Valence Bond Theory, VBT) (10) | 2020.10.27 |
|---|---|
| 화학 전문 용어가 궁금하다면? (0) | 2020.10.19 |
| 무수 아세트산과 아세트산 무수물의 차이 (4) | 2020.10.01 |
| 프랭크-콘돈 원리 (Franck-Condon Principle) (24) | 2020.09.25 |
| 용액의 농도 : 원하는 농도의 용액 만들기 (12) | 2020.09.13 |



