0. 들어가기
대학 시절 유기화학과 분석화학을 정말 못했다. 이렇게 말하면, 마치 물리화학과 무기화학은 잘한 것처럼 오해 할 수 있기 때문에 시작부터 바로 잡아야겠다. 물리화학도 못했고, 무기화학도 그냥저냥이었다.
그럼에도 유기와 분석을 못했던 것이 먼저 떠오른 이유는 내용 이해도 못하고, 잘하고 싶은 욕심도 부족했기 때문이지 싶다. 그냥 한 마디로 하기 싫었던 것 같다. 그에 반해, 물리화학은 나에게 좋고 싫은지, 잘하고 싶은지 판단할 기회조차 주지 않았다. 시작부터 끝나는 순간까지 한결같이 하얀 도화지처럼 깔끔하게 못했고, 어려웠고, 그것은 지금도 마찬가지다.
여기 언급되지 않은 무기화학이 어디까지나 상대적으로 선방했다는 생각이 드는 것은, 앞의 세 과목이 너무 압도적이었던 것이 가장 큰 이유이겠지만, 학부 졸업논문 쓰겠다고 무기화학 실험실에서 2년 동안 생활했던 것이 조금은 영향을 주지 않았을까 싶다.
20대 초반의 까까머리 복학생이 엄청난 프로젝트를 하거나 성과를 남길만한 무언가를 했을 리는 전혀 없다.(지도 교수님께서 그렇게 큰 리스크를 짊어지을 리가 없지 않은가?) 그저 대학원 형, 누나들 사이에서 하루종일 설거지하고, 밑바닥 영어 실력으로 번역기에 의지해가며 논문 읽고, 어리버리하다가 초자류 깨먹고, 졸린 눈 비벼가며 새벽에 출근해서 걸어놓은 반응 날려먹고, 글로는 표현하기 민망한 여러 기타 등등의 사고를 치고, 또 혼나면서 아등바등한 것이 전부다.
당시, 실험실 생활을 하는 동안에는 몸도 힘들고, 뚜렷한 결과도 비젼도 보이지 않아, 내가 뭘하고 있는건가 싶기도 했었는데, 돌이켜 생각해보면 당시에 어깨너머로 보고 듣고 느꼈던 것들이 무기화학 분야의 문턱을 조금 낮게 만들어주고, 익숙하게 여기어 편안함을 준 것이 아닌가 싶다.
주로 금속과 유기리간드 착물에 관한 실험을 주로 했었다. 디스플레이 또는 유기조명용 유기 리간드를 합성하고, 정제하고, 광물리학적 특성을 측정하고, 쓸모 여부를 가려내는 것이 일상이었다. 졸업 논문을 쓰고, 발표를 하던 당시까지도 지식 수준은 크게 달라진 것은 없었음에도, 플라스크 속 합성된(잘 합성되었을 것이라고 믿었던) 착물들과 일방적인 친밀감 정도는 쌓을 수 있었다.
-
졸업하고 학교 현장에 나와보니 화학의 다른 전공 분야에 비해 무기화학 관련 내용은 교실에서 언급될 일 자체가 없고, 여타 활동에 응용하기에도 제한적이다. 화학1의 주기율 단원에서 전이금속은 다루지 않고, 결합 단원에서도 배위 결합은 굳이 소개하지 않으며, 착물(complex)과 리간드(ligand)라는 용어는 교육과정 내 끼워줄 만한 자리가 마땅치 않다.
그럼에도 고등학교에서 무기화학의 일부를 가르치고, 다뤄야 한다고 주장할 생각은 전혀 없다. 고등학생 수준에서 다루어야 할 화학의 여러 세부 영역들 중에는 한참 뒷 순위라 생각한다. 그래서인지, 운좋게 경험했던 과학고에서의 AP 교육과정이나 방과후 시간의 전이금속화학 수업이 소중했고, 당시 학생들 눈에는 수업하는 내가 행복해 보였을 수 있을 것 같다.(아이들이 어려워하고, 고개를 절레절레하는 것에 행복했던 게 아니라고 강력하게 주장한다.)
-
학교에서 학생들과 착물 합성을 시도했던 적이 몇 차례 있다. 대표적인 것은 철-아세틸아세토네이트이다. 붉은색 착물 염료를 합성하는 데 걸리는 시간은 1시간이면 충분하다. 새로운 실험 시도의 대부분은 대학교 일반화학실험 책이나, 무기화학실험 책 등에서 아이디어를 얻는다. 대체로 반응 시간이 짧고, 높은 온도를 요구하지 않으며, 부반응이 적고, 결과를 확인하기 용이한 반응들에 주로 관심을 갖는 편이다. 아,,, 한 가지 더 신경쓰는 것은 실험 후 뒷처리가 쉬워야 하는 것도 학생들과 시도할 지, 말 지를 결정하는 데 중요한 요소이다.
[참고] 금속-아세틸아세토네이트의 합성: https://stachemi.tistory.com/254
금속-아세틸 아세토네이트 착물의 합성
금속-아세틸 아세토네이트 착물의 합성 "Fe(acac)3의 합성 및 분석" 0. 들어가기 겨울방학 중에 진행될 '과학교사 실험연수'에서 강의 일부를 맡게 되었다. 주된 테마가 '심화기기 활용'이라서 어떤
stachemi.tistory.com
그런 면에서 생각하면, Alq3 합성은 최악의 실험이 될 수 있다. 뒷처리의 번거로움 때문에 학교에서는 되도록 하지 않는다. 블로그 방문객의 대다수가 고등학생들이라고 추정하고 있는데, 멋모르고 학교 선생님을 졸라, 무턱대고 했다가 과학실을 엉망으로 만들어버릴까 걱정되어 그동안 공개하지 못했다. 이름 모를 선생님께 민폐끼칠 수 있을 것 같아서 지금도 걱정이다.
이에, 아무 이론적 배경없이 학생들끼리 그저 블로그에 쓰인 대로 용액을 섞고, 가열하고, 거르는 행위는 적극적으로 말리는 바이며, 뒷처리 할 마음가짐과 계획, 여유 시간없이 섣불리 시도하지 않았으면 좋겠다.
Tris(8-hydroxyquinolinato)Aluminum의 합성
OLED의 뿌리를 찾아서...
1. Alq3
IUPAC 이름은 Tris(8-hydroxyquinolinato)Aluminum이며, 간단히 Alq3라 줄여 표현한다. 중심에 위치한 알루미늄 이온(Al3+)이 세 개의 8-하이드록시퀴놀린(8-hydroxyquinoline, 이하 8-HQ)과 배위 결합한 팔면체 착물이다. 8-HQ는 피리딘 고리와 페닐 고리가 인접한 구조를 가지며, 고리의 질소와 산소쪽으로 알루미늄과 결합을 이루며, 8-HQ는 두 자리 리간드(bidentate ligand)로 작용한다.

Alq3는 유기발광다이오드(OLED) 분야에서는 유명한 기초 물질이다. 그리고 이 물질 언급할 때, 빠뜨리면 개인적으로 서운한 인물이 있다. 바로, C. W. Tang(1947- 현재)이다.

1987년 C. W. Tang의 연구팀에 의해 유기 발광 다이오드(OLED)의 저전력·고효율 발광층 소재로서의 Alq3 활용 가능성이 처음 제안되었고, 이후 높은 열 안정성과 뛰어난 전기적·광학적 특성이 밝혀지면서 디스플레이와 조명 같은 응용 분야의 중요 소재로 자리잡았다.[1],[2]
[1] C. W. Tang, S. A. VanSlyke (1987). "Organic electroluminescent diodes". Applied physics letters, 51(12), 913-915.
[2] C. W. Tang, S. A. VanSlyke, C. H. Chen (1989). "Electroluminescence of doped organic thin films". Journal of applied physics, 65(9), 3610-3616.
사실, Tang의 연구 이전에도 안트라센(anthracene) 유기 결정의 전기 자극에 따른 발광(전계발광) 현상이 보고된 바 있었다.[3],[4] 하지만, 유기물에서 발광이 가능함을 보여준 기초 증거 정도로 여겨질 뿐, 기술적 관심 의 대상으로 발전한 것은 아니었다. 그에 반해, Tang의 연구는 현대 유기 발광 다이오드의 기본 구조를 갖춘 최초의 소자를 구현했다는 점에서 의미가 있었고, 그 중심에 Alq3라는 물질이 있었다.
[3] M. Pope, H. Kallmann, P. Magnante (1963). "Electroluminescence in organic crystals". The Journal of Chemical Physics, 38(8), 2042–2043.
[4] W. Helfrich, W. G. Schneider (1965). "Recombination radiation in anthracene crystals". Physical review letters, 14(7), 229-231
2. 이성질체
Alq3는 두 자리 리간드인 8-HQ의 산소와 질소의 배위 결합 배향에 따라 meridional과 facial의 두 가지 이성질체를 갖는다.
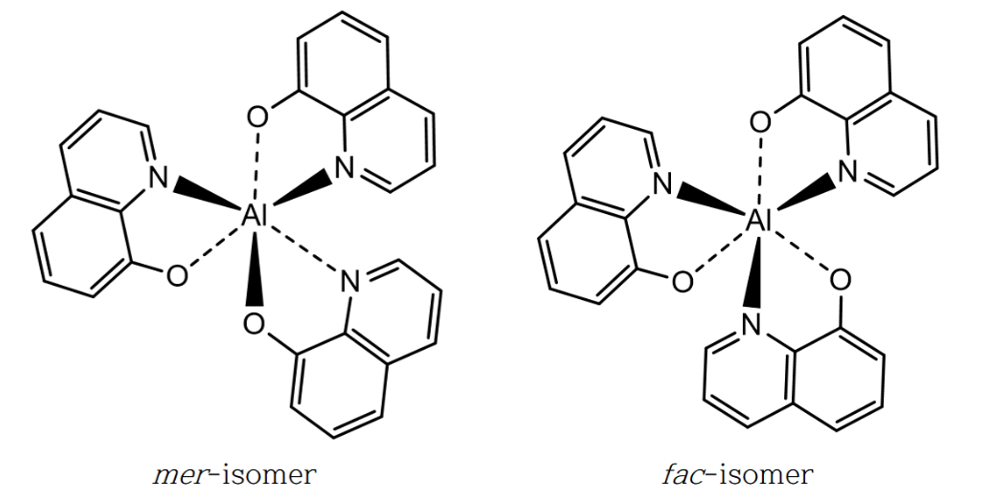
짧은 시간과 낮은 온도에서 합성하는 경우, meridional 이성질체가 주로 생성되며, 고온에서 오랜 시간에 걸쳐 합성해야 facial 이성질체를 얻을 수 있다고 알려져있다. 이는 meridional 이성질체가 facial 이성질체에 비해 전자 분포의 이점을 가져 열역학적으로 안정하고, 속도론적으로도 mer-Alq3가 우세하기 때문으로 설명된다(Curioni et al., 1998; Iwakura et al., 2014).

Alq3를 구성하는 리간드인 8-HQ는 두 자리 리간드로, 질소(N)와 산소(O) 방향으로 금속과 결합한다. 8-HQ는 두 개의 인접한 고리로 이루어져 있는데, 이들 각각의 고리가 착물 전체 에너지 준위에 영향을 미친다. 8-HQ의 피리딘(pyridyl) 고리는 착물의 LUMO, 페닐(phenyl) 고리는 착물의 HOMO 준위 형성에 주된 기여하는 것으로 알려져 있다(Curioni et al., 1998; Muccini et al., 2004; Iwakura et al., 2014).
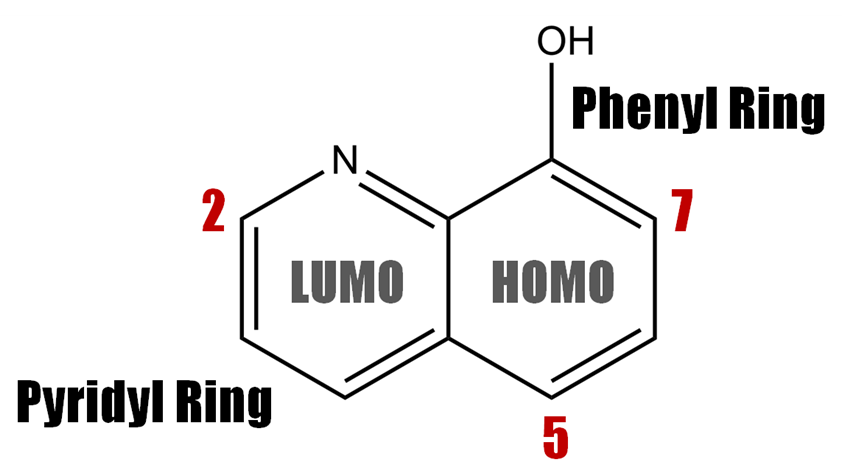
리간드를 구성하는 각 고리가 착물의 HOMO와 LUMO 에너지 준위에 영향을 미친다는 것은 고리에 결합된 수소 자리에 성격이 다른 치환기를 도입하게 되면, 각 고리 내의 전자 밀도 변화가 생기고, 이에 따라 HOMO와 LUMO의 에너지 준위에 변화를 만들어 줄 수 있다는 뜻이기도 하다.
조금 더 자세히 설명하자면, 수소 대신 고리 내 전자 밀도를 풍부하게 만들 수 있는 치환기(EDG)를 도입하거나, 전자 밀도를 감소시킬 수 있는 치환기(EWG)를 도입했을 때, HOMO와 LUMO의 에너지 간격을 조절할 수 있다. HOMO와 LUMO 간격이 달라지면, 흡수 또는 방출하는 빛의 파장이 달라지게 되고, 이에 따라 흡수 및 방출스펙트럼에서 파장 이동(shift)을 관찰할 수 있다.
오래전이지만, 학생들과 이러한 아이디어를 바탕으로 과제연구 활동을 한 적이 있었다. (사실, 새로울 것은 없는 주제이다.) 피리딘 고리의 2번 자리, 페닐 고리의 5번 자리, 7번 자리에 몇가지 전자 끌개 그룹(EWG)과 전자 주개 그룹(EDG)을 각각 도입한 Alq3 유도체를 합성하고, 흡수 파장의 이동을 살펴봤었다. (물론, 학교에서 직접 리간드를 설계하고 합성할만큼의 시간적, 능력적, 환경적 여건이 안되었기에 시중에 판매되던 리간드로만 진행해야 했다는 한계는 있었다.)

2025년 11월, 시그마알드리치(Sigma Aldrich) 기준으로, 질산 알루미늄*9수화물(Al(NO3)3*9H2O)이 100 g에 약 11만원, 8-HQ가 50 g에 약 17만원, 2-methyl-8-HQ가 100 g에 약 9만원, 5,7-dichloro-8-HQ은 100 g에 약 15만원, 5-chloro-8-HQ는 100 g에 약 9만원 정도이다. 그런데 체감상으로는 예전에 훨씬 더 비싸게 주고 구입했던 것 같은 느낌적인 느낌이다.
3. 합성법
고등학교에서 실험실에서 화학, 특히 합성 실험을 진행하기 위해서는 세 가지 정도를 반드시 고려해야 하는데, 첫번째는 안전이다. 그 다음으로 고려할 것이 안전이며, 마지막은 안전해야 한다. (물론, 일반적인 유기 용매나 시약에서 발생할 수 있는 잠재적 위험까지 완전히 배제할 수는 없지만...)
위험 요소가 조금이라도 있는 단계는 최소화할수록 좋다. 지나치게 긴 반응 시간을 요구하거나, 조건이 민감한 단계는 되도록 포함되지 않아야 한다. 과도한 고온·고압 조건이 요구되거나, 반응을 위해 특별한 장치가 필요하면 수행하기 어렵고, 필수로 사용되어야 하는 시약이 너무 비싸면 주머니 사정이 어렵다.
다행인지, (교사에겐) 불행인지 Alq3 합성 과정이 특별히 위험하거나 까다로운 편은 아니다. 산소에 지나치게 민감하여 통제된 환경을 요구하거나 높은 온도, 오랜 반응 시간을 요구하지 않는다. 시약 가격은 학교마다 주머니 사정이 다를테니, 어떻다고 말하기 그렇다. 그러니 넘어가자. 이에, 시약을 확보할 수 있고, 기초 실험이 가능한 실험실 환경이라면 진행 자체에는 어려움이 없다.
다만, Alq3가 물에 잘 녹지 않고, 쉽게 발광한다는 특성이 있기 때문에, 반응을 마친 후, 사용한 유리 기구들을 유기용매(아세톤 등)를 이용하여 깨끗하게 세척하지 않고 제때 정리하지 않는다면, 실험실 곳곳이 얼룩덜룩 노란 흔적으로 뒤덮일 수 있고, 초자류를 볼 때마다 찝찝하게 노란 얼룩이 사라지지 않고 아른거리는 듯한 기분 나쁨을 참아야 할 수 있다. (그래서 아이들에게 굳이 먼저 합성해보자고 제안해본 적이 없고, 학생들끼리 자율적으로 합성해보겠다는 것을 절대 허락하지 않는 편이다. 아세톤으로 초자류를 세척해야만 하는 상황을 만드는 것 자체가 안전상으로도 바람직하지는 않다.)
그래도 누군가는 관심이 생겨 한 번쯤 합성해보고 싶을 수 있기 때문에, 학생들과 과제 연구 당시 참고했던 논문 몇 개로부터 합성법을 옮겨본다. 약간의 차이는 있지만, 결국 알루미늄 이온(Al3+)을 물에 녹이고, 8-HQ도 적절한 용매에 녹인 뒤, 약 1:3의 몰비로 혼합시킨 뒤, pH를 천천히 높여 침전물의 형태로 Alq3 착물을 얻어내는 전반적인 과정은 유사하다.
8-HQ의 물에 대한 용해도(0.5 g/L, 20 ℃)가 작아서 처음부터 에탄올을 용매로 쓰면서 가열하거나, 아세트산을 섞어 쓰는 정도의 차이가 있고, 세부적인 조건과 반응 시간이 조금씩 다를 뿐이다.
합성 과정에서 공통적으로 염기를 천천히 넣으라는(점적, dropwise) 언급이 있는데, 적정 pH 이상 환경에서 Al(OH)3와 같은 원치 않는 부산물(침전)이 생성되는 것을 최소화하기 위한 것으로 보인다. 만약, 농도가 진한 염기를 점적하는 상황이라면, 국소적인 영역에서의 급격한 pH 증가를 막기 위해 비교적 강하게 교반하는 것이 도움이 될 수 있겠다.
가. Li(2003) 합성법[5]
1) 용액 A : 플라스크에 8-HQ 6.97 g(약 48 mmol)과 무수 에탄올 100 mL을 넣고, 적절히 가열-교반 하여 완전히 녹인다.
2) 용액 B : 플라스크에 Al(NO3)3*9H2O 15 g(약 40 mmol)을 탈이온수 200 mL에 녹여 완전히 혼합한다. (원문의 알루미늄 이온의 양이 8-HQ에 비해 너무 과량이다. 5 g(약 14 mmol)의 단순 오타인지, 다른 이유가 있는지, 정확하게는 모르겠다. 알루미늄 이온 : 8-HQ = 1 : 3 정도 몰비로 반응하는 것이 일반적이기 때문에, 개인적으로는 오타인 것 같다.)
3) 용액 C : 플라스크에 NaOH 5.3 g을 탈이온수(물) 60 mL에 녹인다.
4) 용액 A를 B에 천천히 부으면서 완전히 녹을 때까지 교반 한다. 약 15분간 기다리며, 혼합물의 pH는 약 4 부근이다.
5) 용액 C를 [4]의 혼합 용액에 천천히 적가(dropwise)하여 고체 Alq3를 침전시킨다. 최종적으로 pH가 5에 가까워지도록 한다.
6) 혼합물을 24시간 방치한 뒤, 진공 흡착 여과 과정을 수행한다. 탈이온수로 8~10회 세척한 뒤, 진공 챔버에서 150℃ 조건에서 건조하여 밝은 녹색의 Alq3를 얻는다.

나. Mahakhode(2006) 합성법[6]
1) 용액 A : 8-HQ 5 g(약 35 mmol)을 증류수 25 mL와 아세트산 25 mL 혼합물에 녹인다. 오렌지색 투명 용액이 될 때까지 잘 교반 한다.
2) 용액 B : Al(NO3)3*9H2O 4.3 g(약 12 mmol)을 증류수에 녹여 투명한 용액을 만든다.
3) 용액 A와 용액 B를 혼합하고, 10분 동안 지속적으로 교반 한다.
4) 혼합 용액에 암모니아수(NH4OH)를 천천히 방울방울(dropwise) 넣으며 교반 한다.
5) 형성된 노란색-녹색 침전물을 여과한다. 침전물을 증류수로 8~10회 세척하여 잔여 불순물을 제거하고, 자연 건조한다.

다. Katakura(2006) 합성법 (acid-free)[7]
1) 건조한 AlO(OH)를 플라스크에 0.2 g(약 3.3 mmol) 넣고, 8-HQ 1.45 g(약 10 mmol)을 넣고, 물 30 mL를 추가한다.
2) 혼합물을 110 ℃ 오일 배스에서 중탕하며, 환류 장치(reflux condition) 하에서 강하게 교반(stir)한다.
3) 초기 30분 동안 혼합물이 노란색으로 변하며, 24시간 이상 이 색깔을 유지한다.
(반응 시간을 1시간으로 제한하면, 주 생성물로 mer-Alq3 이성질체가 형성되며, 90 시간 동안 환류 교반하면, mer-Alq3가 서서히 fac-Alq3로 전환되어 주생성물이 된다.)
4) 반응이 끝나 생성된 침전물을 차가운 아세톤으로 세척하여 남아있는 8-HQ을 제거한다. 필터를 통해, 정제된 고체 생성물 Alq3를 얻는다. (약 83% yield)

라. Lima(2016) 합성법[8]
1) AlCl3 (1 mol/eq)과 8-HQ (3.5 mol/eq)을 50 mL의 에탄올 수용액(H2O/EtOH(1:1))에 넣고, 60 ℃에서 교반 한다.
2) 완전히 용해된 후, KOH (4 mol/eq)를 물 25 mL에 녹인 염기 용액을 혼합물에 pH 7~8이 될 때까지 천천히 첨가(dropwise)한다.
3) 같은 온도에서 2시간 동안 교반한다.
4) 반응 후 생성된 노란색 침전물을 여과하고, 물, 에탄올, 아세톤으로 여러 차례 세척해 불순물을 제거한다.
5) 최종 침전물을 진공 상태에서 50~80 ℃에서 건조한다. (약 50~80% yield)

마. 참고 문헌
[5] H. Li, F. Zhang, Y. Wang, D. Zheng, "Synthesis and characterization of tris(8-hydroxyquinoline)aluminum", Materials Science and Engineering B, 100 (2003) 40–46.
[6] J. G. Mahakhode, B. M. Bahirwar, S. J. Dhoble, S. V. Moharil, "Tunable photoluminescence from tris(8-hydroxyquinoline)aluminum (Alq3)", Proceedings of ASID ’06 (2006) 237–239.
[7] R. Katakura, Y. Koide, "Configuration-specific synthesis of the facial and meridional isomers of tris(8-hydroxyquinolinate)aluminum (Alq3)", Inorganic Chemistry, 45 (2006) 5730–5732.
[8] C. F. R. A. C. Lima, R. J. S. Taveira, J. C. S. Costa, A. M. Fernandes, A. Melo, A. M. S. Silva, L. M. N. B. F. Santos, "Understanding M–ligand bonding and mer-/fac-isomerism in tris(8-hydroxyquinolinate) metallic complexes", Physical Chemistry Chemical Physics, 18 (2016) 16555–16565.
3. Alq3의 성질
합성한 Alq3 결정은 대체로 밝은 노란색을 띠며, 발광할 때는 녹색 빛깔을 띤다. 마치 노란색 형광펜 고체 분말을 보는 것과 유사하다. 물에는 거의 녹지 않지만, 대부분의 유기 용매(다이클로로메테인 등)에는 비교적 잘 녹는다.

Alq3는 빛(자외선)을 받거나 전기 에너지가 가해졌을 때, 발광(emission)하는 특성을 지닌다. 실험실에 핸드형 자외선 램프가 있다면, 손쉽게 발광 현상을 관찰할 수 있다. Alq3의 발광은 500~530 nm 부근에서 관찰되며, 이는 형광에 해당한다. 형광은 들뜬 전자가 비교적 짧은 시간(10-9~10-8초) 내 바닥 상태로 되돌아오면서 빛을 방출하는 과정이다. 형광(fluorescence)과 인광(phosphorescence)에 대한 자세한 설명은 아래 글에서 확인할 수 있다.
[참고] 형광과 인광: https://stachemi.tistory.com/344
형광과 인광 (Fluorescence & Phosphorescence)
형광과 인광 | Fluorescence & Phosphorescence 안정한 바닥 상태(ground state) 분자가 에너지를 흡수하면, 들뜬 상태(excited state)가 된다. 그리고, 들뜬 상태의 분자가 '빛의 형태로 에너지를 방출'하는 과
stachemi.tistory.com
Alq3의 합성
- 끝 -
* 끝까지 읽어주셔서 감사합니다.
'화학 > 화학이야기' 카테고리의 다른 글
| 농도차 전지와 네른스트 식 (0) | 2025.10.29 |
|---|---|
| 형광과 인광 (Fluorescence & Phosphorescence) (6) | 2025.03.30 |
| 식용색소와 락스 반응을 통한 반응 차수의 결정 (2) | 2024.12.21 |
| 색소의 구조와 종류 (0) | 2024.12.16 |
| DPPH를 이용한 항산화능 분석 (5) | 2024.11.24 |



