형광과 인광 | Fluorescence & Phosphorescence
안정한 바닥 상태(ground state) 분자가 에너지를 흡수하면, 들뜬 상태(excited state)가 된다. 그리고, 들뜬 상태의 분자가 '빛의 형태로 에너지를 방출'하는 과정을 '복사 감쇠'라 한다. 완전 같은 의미라고 할 수는 없지만, 광발광(Photoluminescence)을 떠올리면 된다.
분자가 에너지를 받아 들뜨는 일은 빈번하게 일어날 수 있지만, 들뜬 분자들이 빛 에너지를 방출하는 발광 현상이 그보다 덜한 것은 대체로 들뜸 에너지 대부분이 복사가 아닌 이웃 분자의 진동, 회전, 병진 에너지로 전달되기 때문이다. 이러한 과정은 비복사 감쇠 과정이다.
이번 글을 통해서는 들뜬 상태의 분자가 빛 에너지를 방출하는 복사 감쇠 과정인 형광(Fluorescence)과 인광(Phosphorescence)에 대해 알아보고자 한다.
1. 형광 (Fluorescence)
안정한 바닥 상태(S0) 분자가 에너지를 흡수하면, 높은 에너지의 들뜬 상태(S1)로 전자 전이가 일어난다.
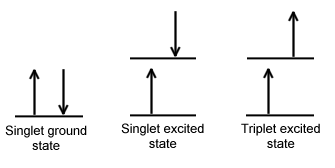
[참고] 바닥 상태와 들뜬 상태가 아랫 첨자 0과 1로 구분된 것이며, 기호 S는 스핀다중도 1의 단일항(Singlet)을 뜻한다.
이 과정은 수직 전이(↑)이다. 수직 전이란, 분자가 에너지를 흡수하여 전자 전이가 일어나 높은 에너지의 들뜬 상태가 되었지만, 결합은 바닥 상태와 같은 길이를 유지하고 있다는 뜻이며, 이러한 전자 전이의 원리를 프랭크-콘돈 원리(Franck-Condon Principle)라 한다.
이후, 들뜬 상태(S1)의 분자는 비복사 감쇠(Radiationless decay, 진동 이완) 과정을 거쳐 들뜬 상태의 최저 진동 준위(S1')에 도달하게 된다. 그리고 이 들뜬 상태의 최저 진동 준위(S1')에서 바닥 상태(S0)를 향한 수직 전이(↓)가 발생하는데, 빛의 형태로 에너지를 방출하는 이 과정을 형광(Fluorescence)이라 한다.

형광은 흡수했던 에너지 일부를 비복사 감쇠 과정(진동 이완)으로 소모한 뒤의 나머지가 방출되기 때문에, 방출 파장이 흡수 파장에 비해 더 긴 것이 보통이다. 이러한 방출 스펙트럼의 장파장 이동 현상을 스토크스 이동(Stokes shift)이라 하며, 형광 염료가 자외선(UV)을 받아 들뜨고, 그보다 더 긴 파장의 청색이나 초록색 가시광선 영역의 빛을 내는 현상이 대표적인 예라고 할 수 있다.

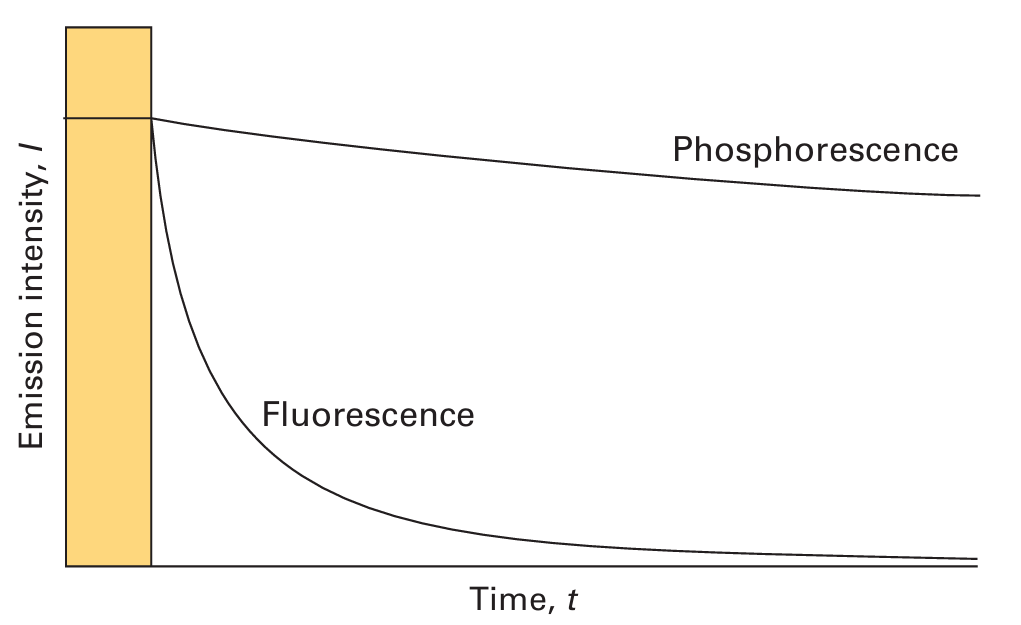
'형광'에서는 전자 들뜸에 기여한 에너지원이 제거되면, 수 나노초(ns) 이내의 짧은 시간만에 빛의 방출이 곧장 일어난다. 그에 반해 후술할 '인광'은 방출 지속 시간이 형광에 비해 장시간(마이크로초에서 수 초내(μs ~ s)) 지속가능하다는 점에서 차이가 있다.
2. 인광 (Phosphorescence)
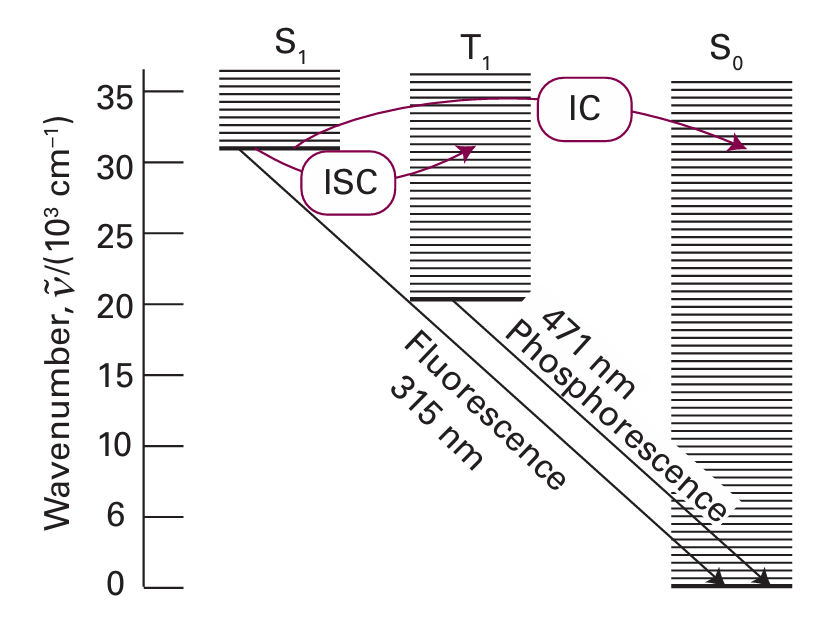
인광도 바닥 상태(S0)의 분자가 에너지를 흡수하여 들뜬 상태(S1)를 향하는 것에는 큰 차이가 없다. 그러나 인광은 들뜬 상태(S1)에서 한 단계를 더 거친다. 바로, 삼중항 들뜬 상태(T1)로의 계간 교차(Inter-System Crossing, ISC) 과정이다. 계간 교차 후, 전자는 형광과 마찬가지로 비복사 감쇠(진동 이완)을 통해 들뜬 상태의 최저 진동 준위(T1')에 도달하게 된다.
[참고] 형광에서와 마찬가지로 바닥 상태와 들뜬 상태는 0과 1로 구분, 기호 T는 스핀 다중도 3의 삼중항(Triplet)을 뜻한다.
일반적으로 삼중항 들뜬 상태의 최저 진동 준위(T1')는 단일항 들뜬 상태의 최저 진동 준위(S1')에 비해 비교적 안정하기 때문에 비복사 감쇠를 거친 전자는 형광에 비해 낮은 에너지 상태(S1' > T1')에 도달한다. 이후, 바닥 상태(S0)로의 전이 과정에서 빛을 방출하고, 이를 인광(Phosphorescence)라 한다.

그런데, 들뜬 상태에서의 계간 교차(S1 → T1)와 들뜬 상태의 최저 진동 준위에서 바닥 상태로의 전이(T1' → S0)는 스핀 금지 전이이다. 두 과정 모두 스핀 다중도의 변화(S=1 ↔ S=3)를 수반하며, 이는 일반적인 상황이라 볼 수는 없다.
[참고] 전자의 스핀 다중도 변화가 없는 전이는 허용 전이이지만, 스핀 다중도가 변하는 전이는 금지 전이이다.
단일항에서 삼중항으로의 전이는 허용되지 않는 것이 분명하지만, 분자의 스핀과 궤도의 커플링(Spin-Orbit Coupling, SOC)이 강하게 이루어질 수 있다면 전이 확률이 높아지는 것으로 알려져 있다. 그리고 이러한 커플링은 원자 번호가 큰 무거운 원소(예: Br, I, Ir 등)가 분자 내 포함되어 있을 때 더욱 효과적이다. (무거운 원소 효과, heavy atom effect)
앞서, '형광'보다 '인광'의 지속 시간이 더 길다고 언급했는데, 이것 역시, 스핀 금지 전이가 발생할 확률이 낮기 때문이라고 볼 수 있다. 어찌어찌 스핀-궤도 커플링에 의해 스핀 쌍이 풀리고, 단일항(S1)에서 삼중항(T1)으로의 계간 교차가 이루어졌다고 해도, 비복사 감쇠 과정 이후, 들뜬 상태 최저 준위(T1')에서 바닥 상태(S0)로 돌아가기 위해서는 또 한번의 금지 전이가 허용되어야 하기 때문이다.
이는 마치, 들뜬 전자들이 계간 교차 과정(S1 → T1)의 힘든 관문을 어찌어찌 통과하여 진동 이완의 강을 건너 들뜬 상태 최저 에너지 준위(T1')에 도달했는데, 또 하나의 힘든 관문(T1' → S0)을 맞이하여, 쉽게 빛으로 방출되지 못하고 해당 지점에 잔뜩 머물러 있는 것과 같다. 이에, 마치 저장고(T1')에 갇혀있던 전자들이 조금씩 조금씩 밖으로 새어나가는 것과 같은 형태로 인광이 나타나며, 형광에 비해 상대적으로 들뜸 에너지가 분자 내에 오랜 시간 저장되어 있는 듯한 차이가 발생하고, 빛의 방출 지속 시간도 길어지게 된다.
3. 참고
- Peter Atkins, Physical Chemistry, 12ed, 11G
- 끝 -
* 끝까지 읽어주셔서 감사합니다.
* 관련글: 144. 프랭크-콘돈 원리: https://stachemi.tistory.com/144
프랭크-콘돈 원리 (Franck-Condon Principle)
프랭크-콘돈 원리 (Franck-Condon Principle) '싸늘하다. 가슴에 비수가 날아와 꽂힌다. 하지만 걱정하지 마라. 전자는 핵보다 빠르니까.' 프랭크-콘돈 원리(Franck-Condon Principle)는 '분광학'과 '양자 화학'
stachemi.tistory.com
'화학 > 화학이야기' 카테고리의 다른 글
| Alq3의 합성 (7) | 2025.11.05 |
|---|---|
| 농도차 전지와 네른스트 식 (0) | 2025.10.29 |
| 식용색소와 락스 반응을 통한 반응 차수의 결정 (2) | 2024.12.21 |
| 색소의 구조와 종류 (0) | 2024.12.16 |
| DPPH를 이용한 항산화능 분석 (5) | 2024.11.24 |



