고등학생을 위한 파동 방정식, 그리고 양자수의 의미
0. 상상하기 쉽지 않은 오비탈 모형, 그리고 양자수
보어의 궤도 모형은 고등학교 교육과정상 물리와 화학에서 비슷한 시기에 다루고, 전자가 핵 주위를 회전하는 모습이 마치, 태양계 행성들을 떠올리게끔 하여 비교적 쉽게 받아들이는 편이다. 하지만, 바로 다음에 등장하는 현대 오비탈 모형은 좀 모호하고 어렵다.
오비탈이라는 단어부터 생소하다. 영단어 orbital만 떼놓고 보면, 보어 모형에서의 orbit(궤도)와 비슷하여 뜻도 비슷하게 생각하면 될 것 같은데, 자꾸 둘은 엄연히 다르다고 하니 미칠 노릇이다.

따라서, 수업을 준비하는 교사 입장에서는 오비탈을 처음 접하는 학생들이 이마를 탁! 칠만한 적절한 비유가 간절하다. 물론, 비유물은 실제 대상을 완벽하게 대체할 수 없고, 때로는 학생들이 비유물과 실제 대상의 모든 면이 똑같다는 착각을 갖게 할 수 있다는 문제점이 항상 남아있기에 아무 비유나 고민 없이 사용하기에 조심스러운 것도 분명하다.
톰슨이 원자의 구조를 플럼 푸딩에 비유했다고 해서 원자에서 자두(plum)맛이 나는 것은 아니잖아?
게다가 2015 개정 교육과정에서는 학생들에게 "양자수와 오비탈을 이용하여 현대 원자 모형(오비탈 모형)을 설명할 수 있다."를 성취 기준으로 요구하면서도 세부 해설을 통해 "각 양자수의 물리적 의미를 강조하지는 않아야 한다."고 제한하고 있기 때문에 심화 내용과 연계하여 설명하는 것에도 제약이 있다. 특히,
"현대 원자 모형에서의 파동함수, 확률 밀도 함수, 확률 분포 함수는 다루지 않는다."
라고 분명하게 다루지 말아야 할 것들을 명시하고 있기 때문에, 함수식이나 그래프를 통한 내용 전개는 아무래도 부담스럽다.
나 역시, 해당 단원 구성의 어려움과 아쉬움 사이를 줄타기하다가, 현재는 간단하게나마 슈뢰딩거의 파동 방정식의 대략적인 아이디어 정도를 언급하고 있다. 왜냐하면, 양자수가 무엇인지는 알아야 왜 그러한 조건을 갖는지, 양자수의 조합에 의해 오비탈이 나타나게 되는지를 받아들일 수 있기 때문이다. (비록, 그 양자수가 갖는 물리적 의미를 굳이 설명하지 않더라도...)
Hψ = Eψ
* 아래 본문에 작성될 내용은 오비탈을 처음 접한 학생들을 대상으로 진행한 수업 스토리에 가까우며, 오비탈과 양자수의 본질적 의미를 설명하는 용어를 쓰기보다는 모호한 개념에 대한 이해에 집중하였기에 실제 의미에서 벗어난 부분들이 여럿 있을 수 있습니다. 이를 감안하여 읽어주시면 감사하겠습니다.
[긴글 주의]
1. 전자는 입자일까? 파동일까?
전자를 얇은 두 개의 구멍(슬릿)을 향해 쏘면 어떻게 될까? 무수히 많은 전자가 두 개의 구멍 중 하나를 통과하여 결과적으로 두 줄을 만들어내지 않을까?
클린턴 데이비슨과 레스터 거머의 이중 슬릿 실험(Davission-Germer experiment, 1927)
학생들은 화학1의 2단원 "원자의 구조" 초반부에서, J.J. 톰슨의 음극선 실험에 대해 배웠다. 진공관에서 나아가는 음극선은 질량을 가졌고 음전하를 나타냈다. 음극선을 이루는 입자의 질량은 당시 알려진 가장 가벼운 입자인 수소보다 약 1800배가량 가벼웠다. (원자보다 작은 입자의 등장!)

결과적으로, 정체가 불분명했던 음극선은 매우 작은 '입자들의 흐름'임이 밝혀졌으며, 우리는 현재 이 입자를 '전자'라 부른다.
음극선의 정체는 바로~~~~~ 음전하를 띠는 매우 작은 '입자'인 '전자'의 흐름이었습니다.
다시 이중 슬릿 실험으로 돌아와서,
전자는 입자이므로 두 개의 슬릿(구멍) 중 하나만 통과할 것이라 쉽게 예상할 수 있다. 따라서 슬릿을 향해 무작위로 쏘아댄 전자 뭉텅이가 슬릿 통과 이후 만들 것으로 기대되는 무늬(결과)를 아래 그림 중에 고르라고 했을 때, (a)라고 답하는 것이 전혀 어색하지 않다. 왜냐하면, 전자도 '입자'이니까!
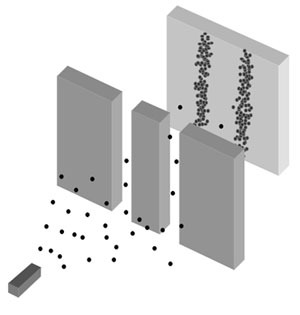

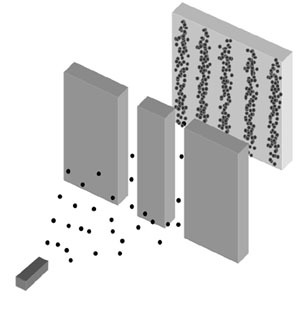
그러나 이중 슬릿 실험 결과는 우리의 예상을 한참 뛰어넘었다. 그림의 (c)처럼 여러 줄의 간섭무늬가 나타난 것이다. 간섭 무늬는 (b)와 같은 파동이 만드는 대표 현상이며, 간섭무늬가 만들어졌다는 사실은 쏘아진 무언가가 파동이었음을 뒷받침하는 강력한 증거가 된다.

예상밖의 결과가 아닐 수 없다. 음극선 실험 결과에 의하면 전자는 분명 입자다. 입자임을 뒷받침하는 증거가 분명하게 있다. 전자는 두 개의 슬릿 중 하나만 선택적으로 통과해야 하는데, 어떻게 간섭무늬가 만들어질 수 있다는 것인가?
알고보니 전자는 입자가 아니었나? 어떤 착오로 인해 잘못 알고 있었나? 지금껏 알려진 입자성을 뒷받침하는 실험 결과들에 잘못된 해석이 있던 것인가? 전자의 정체는 입자가 아닌, 파동이었던 것인가?
적어도 이중 슬릿 실험 결과만 떼어보면, 전자는 파동이라 생각하는 것이 보다 타당해 보이긴 한다.
-
고등학교 2학년 학생일지라도 입자와 파동에 대해 개념이 모호한 경우가 훨씬 많다. 파동이 동시에 두 슬릿을 통과한다는 부분을 쉽게 받아들이지 못하는 경우도 종종 있다. 입자와 파동에 대한 이해를 돕기 위해 교실 앞문과 뒷문을 동시에 열고 일부러 복도로 나간다. 그리고, 교실을 향해 크게 소리친다. (수업 중인 다른 반에 민폐인 것은 분명하지만, "야이~~~~~~~삐리리야!" 소리치고, 아무렇지도 않다는 듯 교실로 들어와 설명을 이어나간다.)
"만약, 내 목소리가 입자였다면, 앞문과 뒷문 중 한 곳으로만 통과하여 학생 누군가의 귀에만 도달했겠지만, 다행히도 파동의 성질을 갖기에 앞문과 뒷문을 동시에 통과하여 여러 학생에게 한꺼번에 전달될 수 있었습니다. 만약, 목소리가 입자였으면, 수업을 위해 학생 한 명 한 명에게 각각 수업 내용을 전달해야 했을 것입니다. (휴, 정말 파동이어서 다행이다.)"
다시 학생들에게 질문해본다. 전자는 파동이니? 입자이니?
-
파동이라면, 음극선 실험에서 관찰된 결과는 어떻게 설명한단 말인가?
입자라면, 이중 슬릿 실험에서 관찰된 결과는 어떻게 설명할 수 있단 말인가?
2. 그런데... 파동이면서 입자일 수도 있지 않음?
사실, 전자는 파동이면서 동시에 입자인 것은 아닐까? (무슨 말같지도 않은...)
'파동임? 아님, 입자임?'과 같은 논쟁은 사실, '전자' 대상으로 처음 발생한 것은 아니었다. '빛(light)'이 먼저였다.
아이작 뉴턴은 빛을 '입자 다발'이라 생각했다. 하지만, 이후 쏟아지는 여러 파동의 증거를 반박하지 못했고, 과학계에서 빛은 '파동'이라고 여겨지는 것이 일반적이었다.
그러던 중, 빛이 완전한 파동이라면 설명하기 어려운 광전효과(photoelectric effect)라는 현상이 관찰되었고, 이를 설명하기 위한 아인슈타인의 광양자설(1905)이 등장했다. 이후, 콤프턴 산란 실험(1922) 결과는 아인슈타인의 생각을 뒷받침해 주었고, 빛은 입자성과 파동성을 모두 가질 수 있는 특별한 지위를 갖게 되었다.
빛도 그렇다매? 그렇다면, 전자도 그런 것 아님? 처음이 어려운거지... 뭐... 꼭, 빛만 그러라는 건...
- 루이 드 브로이, 1892-1987
사실, 바로잡아야 할 것이
위에서 먼저 제시했던 데이비슨과 거머의 이중 슬릿 실험 전자편(1927)은 "입자임이 분명한 전자가 동시에 파동성을 가질 수 있는지를 '확인'하기 위한 실험"이었다. 이 실험에 대한 아이디어는 3년 전인, 1924년에 발표된 드 브로이의 박사학위 논문 『양자론에 대한 고찰』에 '물질파 이론(matter waves)'으로 실려있었다.
닐스 보어는 원자 내부를 설명하기 위해 '궤도 모형'을 제안했다. 자신의 모형을 제안하는 과정에서 "전자는 특정 궤도를 원운동하며, 허용된 궤도를 회전하는 전자들은 전자기파를 방출하지 않는다."라고 대담하게 가정했는데, 드 브로이는 입자인 전자가 파동의 성질을 동시에 가질 수 있다면 보어가 제안한 가정에 담긴 물리적 의미를 설명할 수 있을지도 모른다고 생각했다.
-
드 브로이 말대로, 전자가 입자인 동시에 파동성을 갖는다면, 전자라는 입자에도 파장(λ )이라는 물리량이 표현되어야 한다. 파동(wave)에는 진폭(amplitude)이 있고, 파장(wavelength)이 있다. 그렇다면 전자의 파장은 얼마인가?
"전자는 원궤도에 묶여 진동하는 끝이 막힌 파동(정상파, standing wave)이 아닐까?"
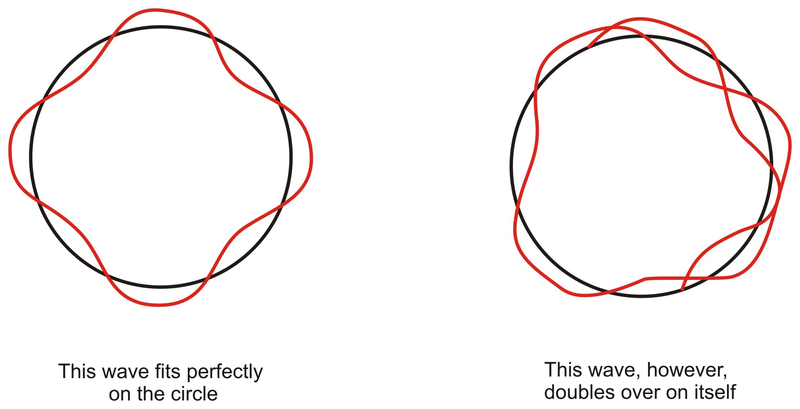
전자가 정상파라면, 원형 궤도의 둘레(= 2πr )가 파장의 정수배(= nλ )될 때는 허용되지만, 정수가 아니면 파동의 시작 지점과 끝지점이 만나지 않고, 파동이 소멸되어 원형 궤도가 허용되지 않는다.
즉, 원 궤도의 둘레 길이가 파장의 정수배를 만족해야만 허용되고, 허용된 파동만이 원자 내에 남을 수 있다. 따라서 원자 내에 허용되는 파동은 n = 1, 2, 3 ... 등의 정수로 구분될 수 있다.
-
보어는 n = 1, n = 2 등의 n = 정수인 궤도에는 전자가 존재할 수 있지만, n = 1.58과 같이 조건을 만족하지 않는 궤도에는 존재할 수 없음을 가정했다. 원자 스펙트럼이 선의 형태로 나타나는 것을 설명하려면, 전자는 불연속적인 에너지 값만을 가져야만 하는데, 그래야만 하는 (그럴듯한) 이유를 만들어주지는 못했다.
그런데, 드 브로이가 '전자가 정상파 조건을 만족하기 위해서는'이라는 이유를 만들어 줄 수 있게 된 것이다. 드 브로이가 제안한 정상파 조건에 보어가 제시한 양자수 조건을 조합하면 더더욱 놀라움을 가져다 준다.
* 보어의 양자수 조건 : 전자의 각운동량(mvr)은 플랑크 상수(h/2π)의 정수(n)배이다 → mvr = nh/2π
* 드브로이의 정상파 조건 2πr = nλ
결과적으로 정리된 수식에는 파동의 물리량인 파장(λ)과 입자의 물리량인 운동량(p = mv )이 함께 나타나는 형태를 갖는다. 운동하는 입자와 파장에 대한 관계식이라니...
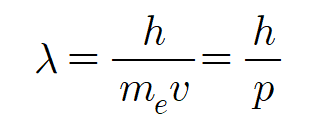
3. 전자의 파동성을 수학으로 나타낸다면?
정말, 전자라는 입자가 파동성을 동시에 갖는다면, 전자의 파동은 어떤 수식(방정식)으로 표현될 수 있을까? 이러한 관점에서 전자를 설명하고자 했던 인물이 (고양이가 더 유명한) 에르빈 슈뢰딩거이다. 슈뢰딩거는 전자의 파동성에 주목하였으며, 전자의 파동성을 나타낼 수 있는 파동 방정식을 고안했다.
전자의 파동성을 나타낸 수식은 어떤 형태일까?
y = ax + b ? 아니다 이건 파동의 방정식이 아니라 직선의 방정식이다. 생각을 반대로 해보자. 우리가 일반적으로 파동이라 생각하는 것들을 수학으로 나타내면 어떤 형태를 갖는가?
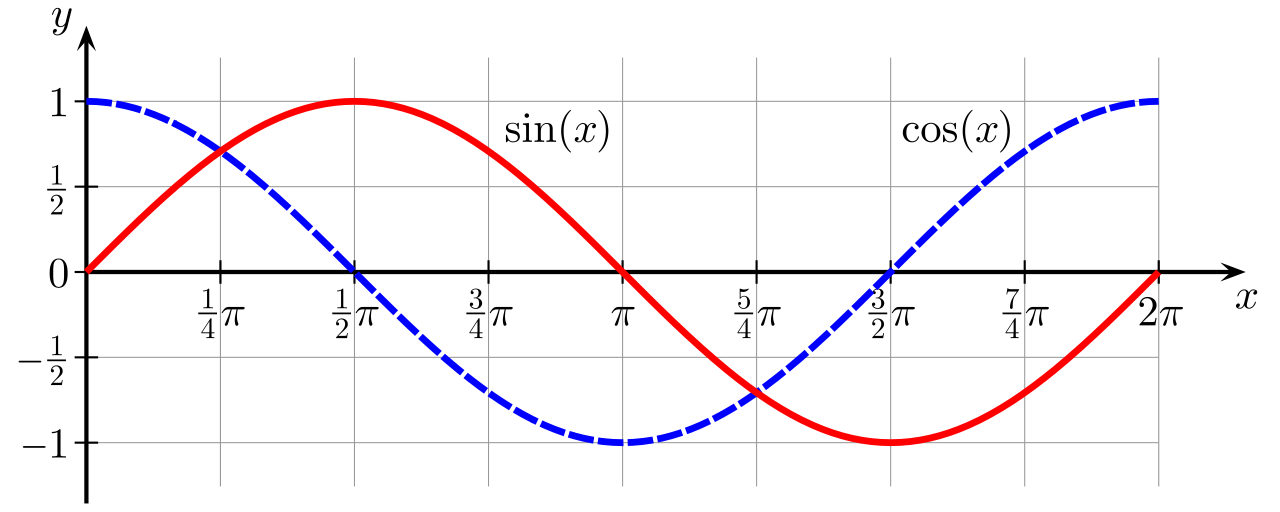
만약, 전자가 파동성을 갖고, 전자가 파동이라면, 그 수식의 형태는 어쨌든 우리가 알고 있는 일반적인 파동의 것과 비슷한 형태를 가져야 할 것이다. 그렇다면, 일반적인 파동은 수학적으로 어떻게 표현되는가?
y = a sin x ? , y = b cos x ?
우리가 전자의 파동에 관한 수식은 이것이다라고 정확하게 표현할 수 없어도, 결국은 sin 또는 cos 또는 이들이 조합된 형태를 가질 것이다. 전자가 파동이라면, 그 파동을 수학으로 표현한다면 그러할 것이다.
그렇다면, sin 함수와 cos 함수가 가지고 있는 수학적 성질들이 '전자의 파동 수식'에도 그대로 나타나지 않을까?
그렇다면, sin, cos 함수가 갖는 독특한 수학적 성질엔 무엇이 있을까? 파동을 나타내는 함수식이 다른 함수들과 구분되는 명확한 성질이 있다면, '전자의 파동 수식'에도 그러한 수학적 성질이 나타날 텐데...
sin x를 미분하면, cos x, 이를 한 번 더 미분하면, - sin x
cos x를 미분하면, - sin x, 이를 한 번 더 미분하면, - cos x
1) 그렇다! sin 함수와 cos함수를 두 번 연속 미분하면, 이전과 달리 앞에 음의 부호가 붙고 상수값이 달라지긴 하지만, 결국 최초의 sin과 cos 함수 형태가 돌아온다. 따라서 2) 어떤, 파동에 대한 수식을 두 차례 연속으로 미분하면, 자기 자신의 최초 파동에 대한 수식 형태(sin 또는 cos)가 그대로 남아있다는 뜻이다.
정리하면, 3) 전자가 파동이고, 전자의 파동성을 표현하는 어떤 수식(Ψ)에 연속 두 번 미분하는 연산을 취하면(H, operator, 연산자), 앞에 어떤 상수항(E, eigen value, 고윳값)과 원래 수식(Ψ)이 곱해진 특징을 가질 것이다. 이를 방정식 형태로 간단하게 나타내면 다음과 같다.
H Ψ = E Ψ
"파동에 관한 함수식(Ψ)에 어떤 명령(H )을 내리면, 특정 값(E )과 함께 자신의 원래 함수식(Ψ)이 남는다.
이것은 파동함수가 갖는 고유한 수학적 특징이다."
4. 그래서 전자의 파동함수 식은 어떻게 생겼어요?
이쯤 되면, (어쩌면) 파동함수 식(Ψ)이 어떻게 생겼을지, 궁금해질 수 있다. 파동함수 식이 Ψ = ax + b, 아니 Ψ = a sinx 정도만 되어도 공부할 마음이 마구마구 샘솟았겠지만, 현실은 차갑고 냉정하다.
양성자 1개, 전자 1개로 이루어진 가장 간단한 원자인 수소의 파동함수 식도 상당히 복잡하다. (아. 싫다. 구하는 과정도... 어렵... 나도 잘 모르고...)
[참고] 수소꼴 원자의 슈뢰딩거 방정식 풀이 (1) https://stachemi.tistory.com/73
[참고] 수소꼴 원자의 슈뢰딩거 방정식 풀이 (2) https://stachemi.tistory.com/74
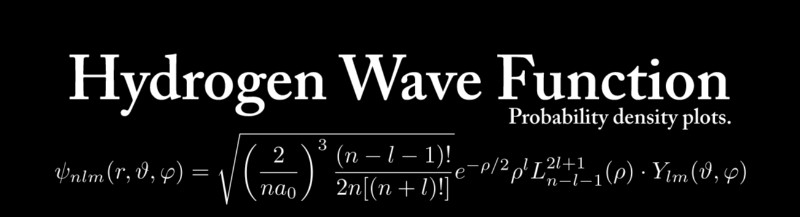
식을 자꾸 쳐다보면 어지럽고 현기증이 날 수 있으니, 쳐다보지 말자. 반드시 실제 식을 통해 내용을 이해해야 할 필요는 없다. 그냥 위의 복잡한 식을 다음과 같이 바꾸어 생각해 보자.
1) 파동함수 식 Ψ = @n#$%&l *m 가 파동 함수 조건을 만족하기 위해서는 어떤 조건들이 필요할까?
2) y = ax + b 가 1차 함수 조건을 만족하기 위해서는 수식에 어떤 조건들이 필요할까?
위의 1)의 경우, 고등학생 수준에서(아니 나이와 관계없이 대부분) 도무지 설명할 구멍이 보이지 않지만, 2)의 경우는 교실 속 학생들 중에도 몇몇이 상수 a와 b가 갖추어야 할 조건에 대해 곧잘 대답한다.
"일단, a ≠ 0 이어야 해요. 0이면 1차 함수가 안 돼요."
"그렇다면, b는 어떤 조건이 필요하죠?"
"음... b는 다 되지 않나요?"
위의 2) 식이 1차 함수 조건을 만족시키기 위해 a와 b가 갖추어야 할 조건, 허용되는 값이 있는 것처럼, 1)식의 Ψ도 파동성을 나타내는 함수식(파동함수 식)이 되기 위해 선행되어야 할 조건이 있고, 조건에 해당하는 값이 있다. 이 조건들을 양자수(quantum number)라 한다고 설명한다.
1차 함수식에 상수에 해당하는 a와 b가 만족해야 할 조건이 있는 것처럼 파동 함수식에는 세 가지 양자수 n, l, ml 이 있다. 각각의 조건은 다음과 같다.
"첫 번째 양자수인 n 은 1, 2, 3 등의 자연수여야 합니다.
두 번째 양자수 l 은 n - 1까지의 음이 아닌 정수를 모두 가질 수 있습니다. 전체 l 의 개수는 결국 n 값에 의존합니다.
마지막 양자수 ml 은 - l 부터 + l 까지의 정수를 가집니다. 역시 가질 수 있는 전체 ml 의 개수는 l 값에 의존합니다."
정리하면, 양자수는 전자의 파동성을 나타내는 수식(Ψ)이 파동의 수학적 형태를 갖추기 위해 갖추어야 하는 조건이라고 할 수 있다. 당연히 양자수들의 조합 (n, l, ml)이 달라지면, 수식의 형태가 달라질 것이고, 표현된 파동의 형태 또한 달라질 것이다. (y = x 와 y = 2x + 1 가 다른 것 처럼)
-
그리고, 이러한 다양한 양자수의 조합들에 의해 나타난 수식, 허용된 파동함수식을 오비탈(orbital)이라 한다.
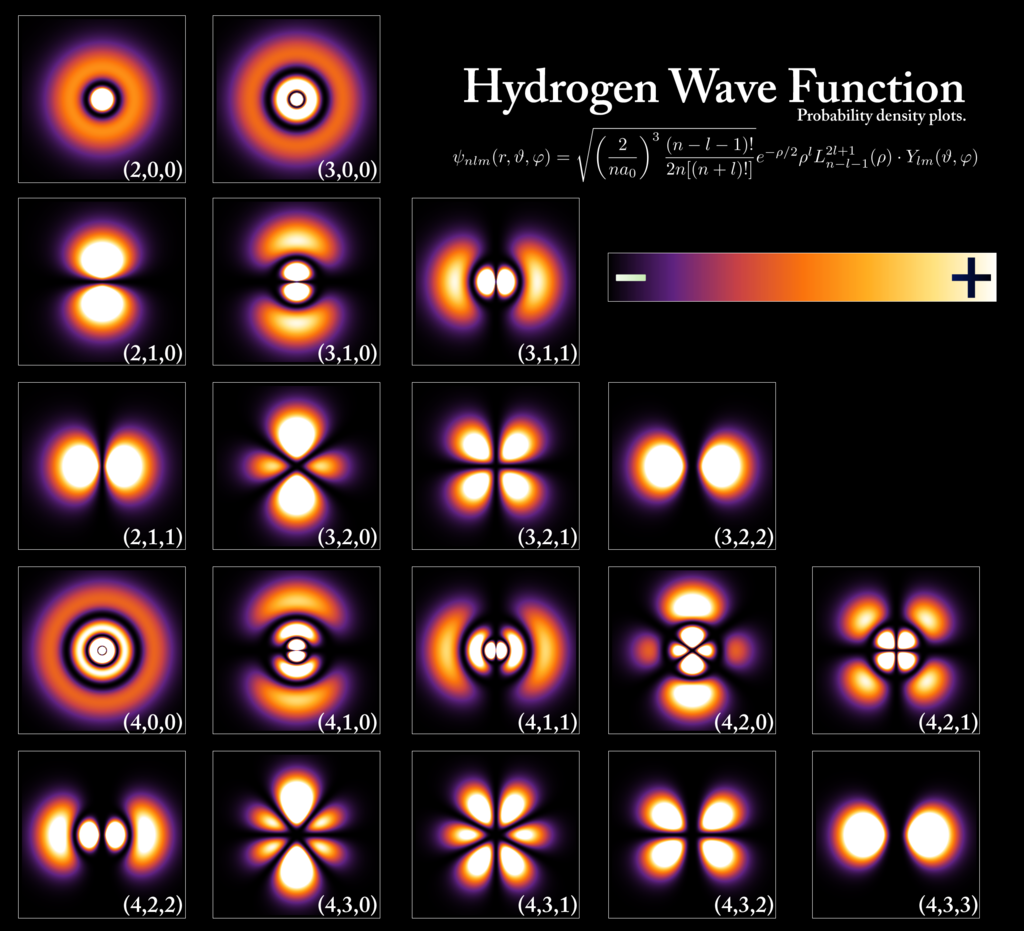
- 끝 -
* 긴 글 읽어주셔서 감사합니다.
[관련 글] https://stachemi.tistory.com/121
현대적 원자 모형 : 오비탈과 양자수
* 본문 내용은 고등학교 화학1을 공부하는 학생을 대상으로 작성한 글입니다. 최대한 파동함수 언급 없이 오비탈 개념을 설명하다 보니 본질에서 벗어난 비유적 표현/용어들이 사용되었음을 감
stachemi.tistory.com
[관련 글] https://stachemi.tistory.com/314
데이비슨-거머 실험 (Davisson-Germer Experiment)
데이비슨-거머 실험 너는 좋은 사람이야? 아니면 나쁜 사람이야? 1927년 미국 물리학자인 클린턴 데이비슨(Clinton J. Davisson, 1881-1958)과 레스터 거머(Lester H. Germer, 1896-1971)는 루이 드 브로이가 제안
stachemi.tistory.com
'화학 > 화학이야기' 카테고리의 다른 글
| 지시약의 pKa 결정 (feat. 분광광도법) (0) | 2024.05.09 |
|---|---|
| 데이비슨-거머 실험 (Davisson-Germer Experiment) (1) | 2024.01.27 |
| [리뷰] "끼리끼리 녹인다." 개념을 가르치기 위한 용매 추출 시범 실험 (0) | 2023.08.04 |
| 분자 요리 (Molecular Gastronomy) (0) | 2023.07.14 |
| 평형 이동과 공통이온효과 (2) | 2023.06.05 |



