2023학년도 고3 3월 학력평가(서울특별시교육청) 국어 지문을 내 스타일대로 재작성해 보았다.(화학 풀이보다 재미있다.) 대부분은 문맥을 고치지 않으려 노력했으나, 작성하다보니 내 호흡에 맞춰 끊거나 내용을 첨가한 부분이 여럿 있다.
관련 이론을 모르는 채로 그림도 없이 글만 읽고, 완전하게 이해했다면 물리와 화학에도 재능이 있어 보이니 진지하게 관련 진로도 고려해 주길 부탁한다. 세부적인 지식은 많이 부족하지만, 내가 아는 화학 범위 내에서 풀어서 서술해 보았다. 다행히도 14 ~ 17번 문제는 풀고 답을 확인해 보았는데 다 맞긴 했다. (휴~)
1. 용해도와 결정화
용해도(solubility)는 일정한 온도에서 일정한 양의 용매에 최대로 녹을 수 있는 용질의 양으로, 보통 용매 100g에 녹을 수 있는 용질의 질량이다. (실제 지문에 오타가 있는 듯하다.)
용매(녹이는 물질, solvent) + 용질(녹는 물질, solute) = 용액(solution)
혼합물의 과포화 상태(supersaturation)란, 용질이 용해도 이상으로 녹아있는 상태를 말한다. 어떤 혼합물이 과포화 상태에 놓이면, (과하게 녹아있는 용질을 뱉어내고) 포화 상태로 돌아가려는 경향이 있다.
결정화(crystallization)는 포화 상태였던 혼합물이 (온도의 하강 등의 요인으로 인해 용해도가 작아지고) 과포화 상태에 놓이게 되어 용질이 고체 입자로 석출 되는 것을 말하는데, 결정화 공정을 거치면 입자 하나하나의 평균 지름(입도)이 작은 고체(고운 가루 형태의 고체)를 얻을 수 있다. 이러한 결정화 공정은 약물의 생체 흡수율을 높일 필요가 있는 제약 분야에서 활용된다.
2. 결정화 공정에서 사용되는 초임계 유체란?
결정화 공정에서는 초임계 유체(supercritical fluid)를 쓰는 경우가 많다. 물질은 어떤 온도와 압력 조건(임계 온도, 임계 압력) 이상에서는 더 이상 액체 또는 기체로 정의될 수 없는데, 이러한 상태를 초임계 상태라 한다.
임계 온도(Tc)는 어떤 물질이 액체로 존재할 수 있는 최고 온도이고, 입계 압력(Pc)은 어떤 물질이 기체로 존재할 수 있는 최대 압력을 말한다. 온도와 압력이 임계 온도와 임계 압력 이상일 때 물질은 액체도 아니고, 기체도 아닌 초임계 상태로 존재한다.

초임계 상태 물질의 분자 사이 거리는 기체 상태일 때보다는 가깝지만, 액체가 될 정도로 가까운 것은 아니다. 어떤 물질이 액체일 때보다는 초임계 유체나 기체 상태일 때, 그 속의 용질이나 용매가 더 자유롭게 움직일 수 있으며, 초임계 유체에 가해지는 압력을 높이면 그 속에 더 많은 양의 용질을 녹일 수도 있다.
따라서 초임계 유체를 이용한 결정화 공정에서는 고체 입자의 평균 지름(크기)을 조절할 수 있다.
3. 결정화 공정 (1) GAS 공정
GAS 공정에서는 초임계 상태의 이산화탄소(CO2)를 반용매로 사용해서 혼합물에 녹아있던 용질을 작은 크기의 고체 입자 상태로 석출 하는 경우가 많다. 여기서 반용매란, 첨가되었을 때, 용질은 녹이지 않으면서 기존 용매와는 잘 섞일 수 있는 물질을 말한다. 반용매를 혼합물에 첨가하면, 반용매와 용매는 섞이지만, 반용매와 섞이지 못하는 용질은 고체 입자로 석출 된다.
GAS 공정에서는 결정화하려는 대상 물질을 액체 용매에 녹여 혼합물을 만들어 용기에 적당량을 넣고, 밀폐한다. 이후 용기의 온도와 압력을 이산화탄소와 액체 용매의 임계 온도와 압력 사이에 맞추고, 초임계 이산화탄소를 주입한다. 그러면, 혼합물은 과포화 상태가 되고, 용질이 고체 입자로 석출 된다. 반용매(이산화탄소)가 용매와 섞이면서 포화될 수 있는 용질의 양이 줄어드는 것이다. (반용매인 이산화탄소가 용매와 상호작용하면서, 용질-용매 사이 상호작용을 방해하고, 용질이 녹는 것을 방해한다고 볼 수 있다.)
* 위의 기울임으로 나타낸 부분을 좀 더 이해하고 싶어서 GAS 공정이 어떤 단어의 줄임말인지 찾아보려 했는데, 검색결과가 마음에 들지 않는다. gas anti-solvent가 제일 유력해보이는데, SAS(supercritical anti-solvent) 공정으로 더 많이 검색된다. 같은 공정에 대한 표현 차이인지, 다른 세부적인 차이가 있는지 나는 잘 모르니 패스~
4. 석출과정에서 입자의 크기와 양을 결정짓는 요인
석출 되는 용질의 양은 처음에 채운 혼합물의 전체 양이 같다면, 그 농도에 따라 결정된다.
결정화 공정에서 고체 입자를 석출 될 때는 우선 일정한 개수 이상의 용질 분자가 모여서 만들어진 결정핵이 생성되어야 한다. 혼합물의 농도가 높을수록 결정핵을 만들 수 있는 용질 분자 수가 많아 결정핵이 많이 생길 수 있다.
하나의 용액 안에서 결정핵이 동시에 많이 생긴다는 뜻은 결정핵 주위에 모여 입자의 크기를 키울 수 있는(결정을 성장시킬 수 있는) 용질 분자 수가 적어진다는 뜻이기도 하며, 고체 입자의 크기는 평균적으로 작아지게 된다.
5. 결정화 공정 (2) RESS 공정
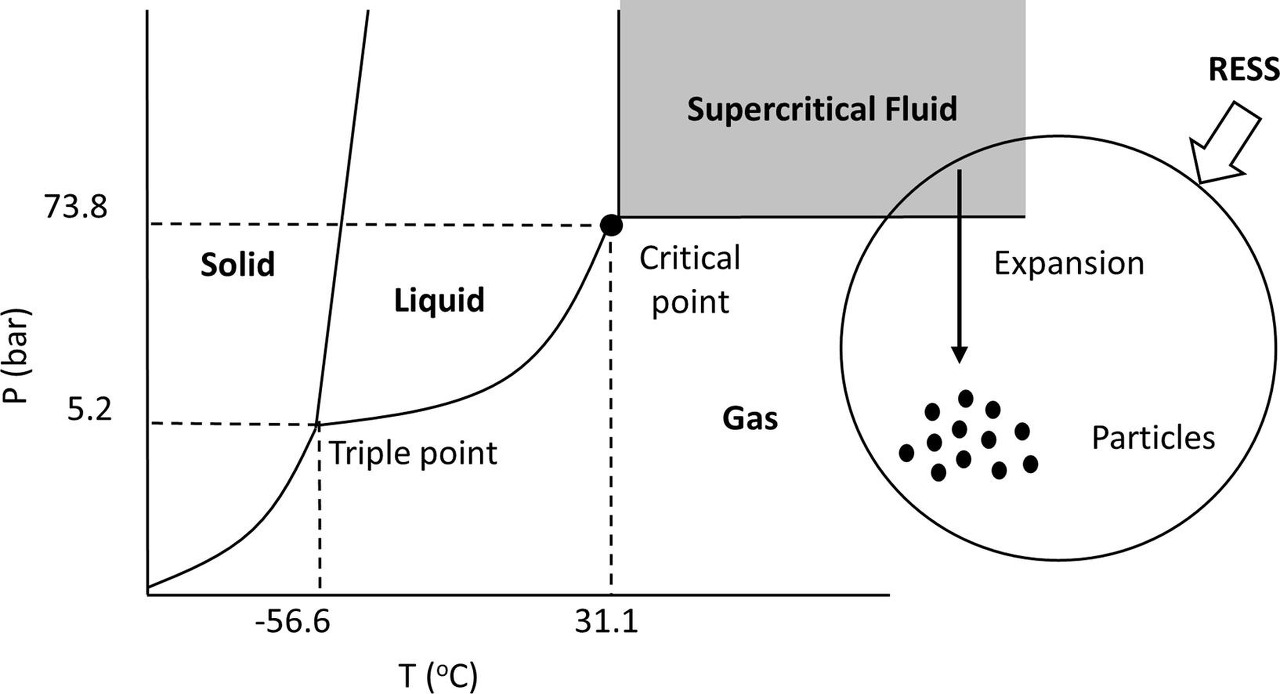
한편, 초임계 이산화탄소를 용매로 사용하는 결정화 공정도 있다. RESS 공정에서는 결정화하려는 물질과 초임계 이산화탄소가 섞인 혼합물을 고압의 용기에서 대기압의 용기로 분사한다. 분사 직후에 초임계 이산화탄소는 압력이 빠르게 임계압력보다 낮아지게 되고, 기체 상태로 변하게 된다. 이 과정에서 용질이 고체 입자로 석출 된다.
* RESS 공정은 Rapid Expention of Supercritical Solution 공정의 줄임 표현인듯 하다.
이때 혼합물에서 결정핵이 생성되는데, 고체 입자의 크기가 정해지는 원리는 위의 GAS 공정과 같다.
6. 결정화 공정에서 이산화탄소를 사용되는 이유
GAS 공정과 RESS 공정 등의 결정화 공정에서는 이산화탄소가 주로 쓰인다. 그 이유는 이산화탄소의 임계 온도(31.05℃)와 상온(25℃)에 큰 차이가 없어서 온도와 압력을 조절하면, 쉽게 초임계 상태로 만들 수 있기 때문이다. 초임계 이산화탄소를 이용하면, 압력을 조절하여 석출 되는 고체 입자의 크기를 작게 만들 수 있을 뿐만 아니라 이산화탄소 그 자체로는 독성이 없어서 안정성 문제에도 자유롭기 때문이다.
* 출처는 2023학년도 3월 고3 전국연합학력평가 국어영역 14~17번 문항에 해당하며, 원문은 서울시교육청과 EBSi 사이트에서 확인할 수 있습니다.
* 임계점(critiacl point)에 대한 설명은 https://stachemi.tistory.com/46
상평형 그림(Phase Diagram)
상평형 그림(Phase Diagram) 1. 상(Phase) 상(Phase)이란, 물질의 화학적 조성과 물리적 상태가 전체적으로 균일한 상태를 말한다. (완전히 혼합된 기체 혼합물이나 완전히 혼합되는 두 액체가 만드는 용
stachemi.tistory.com
'화학 > 기출풀이' 카테고리의 다른 글
| 2024학년도 수능 6월 모의평가(2023.6.1.) 화학1 3점 문항 풀이 (0) | 2023.06.07 |
|---|---|
| 2024학년도 수능 6월 모의평가(2023.6.1.) 국어 지문 [8~11번] (0) | 2023.06.01 |
| 2022학년도 10월(10.12.) 고3 전국연합학력평가 화학1 3점 문항 풀이 (0) | 2022.12.15 |
| 2022학년도 10월(10.12.) 고3 전국연합학력평가 화학1 풀이 [20번] (0) | 2022.12.15 |
| 2014학년도 3월(3.12.) 고3 전국연합학력평가 화학1 풀이 [20번] (0) | 2022.10.27 |



