2014학년도 3월 고3 전국연합학력평가 문제 풀이 [20번]

정답 : ⑤ ㄴ, ㄷ
풀이 :
일정 온도, 압력 조건에서 반응 전후의 부피 비가 피스톤 높이로 주어져있다. 피스톤의 부피는 용기 내 존재하는 기체 분자의 몰 수에 비례한다. 화학 반응식의 양적 관계 문제이다.
(가)의 반응 전 기체 입자 수를 통해 몰 수와 부피 관계를 알 수 있다. 4 mol에 해당하는 부피가 8 부피이다. 1 mol 당 2 부피씩 차지한다.
기체 분자 1 mol = 2 부피
따라서 (가)의 반응 후 남아있는 기체 몰수는 7 부피에 해당하는 3.5 mol이다. 같은 방법으로 (나)의 반응 전 기체 몰수는 8부피에 해당하는 4 mol이며, (나)의 반응 후 기체 몰수는 6 부피에 해당하는 3 mol이다.
(가), (나) 모두 반응 전보다 반응 후의 부피가 줄었다. 이는 화학 반응식에서 반응물 계수 합보다 생성물의 계수 합이 더 작다는 뜻이다.

만약, 반응 전 후의 계수 합이 같다면, 한계 반응물의 종류에 관계없이 반응 전후 부피(입자수)는 변하지 않는다. 남아있는 물질은 어차피 반응 전에도, 반응 후에도 있었기 때문에 변화의 고려 대상이 아니다.
<보기>를 살펴보면,
ㄱ.
X는 이원자 분자일까? 위 반응을 화학반응식으로 나타내면 다음과 같다. (사실, 이 문제를 풀어낼 때, 다음의 화학 반응식을 세우는 것이 가장 핵심이다. A2aB2b 형태로 세워도 결과는 같지만 과정이 조금 지저분하다.)

만약 X가 AB 타입의 이원자 분자라면, 계수 a 와 b 는 모두 1이며, 반응 전후 계수 합의 차이가 없어지기 때문에 문제와 같은 피스톤의 부피 변화가 나타날 수 없다. 따라서 ㄱ 보기는 거짓이다.


ㄴ.
(가)와 (나)의 한계 반응물은?
(가)와 (나) 모두 반응 전 4 mol 임은 동일하지만, 비율이 다르다. (가)는 A2가 1 mol, B2가 3 mol, (나)는 A2, B2 모두 2 mol 씩이다.
같은 4 mol이 반응했음에도 반응 후에 (가)보다 (나)의 부피가 더 작다는 것은 반응이 진행된 후 만들어진 생성물 X의 양이 (나)가 더 많다는 뜻이다. 왜냐하면, 반응물의 계수 합보다 생성물의 계수 합이 작기 때문에 (a + b > 2) 생성물이 많이 만들어질수록 반응 전보다 부피가 크게 감소한다.
반응 (가)에서 B2가 한계 반응물이라면? 3 mol의 B2가 모두 소진되고, A2는 1 mol보다 작은 양이 반응에 참여한다. 그렇다면, (나)에서는 반응전 B2의 양이 2 mol로 줄었기 때문에 무조건 (가)보다 생성되는 X의 몰수는 줄어들 수 밖에 없다. 그러나 (나)의 반응 후 부피는 (가)보다 작고, 위 가정이 잘못되었음을 말한다.
따라서 (가)에서 한계 반응물은 A2이다. (가)에서 A2 1 mol이 모두 소진되고, B2가 남는다. B2가 몇 몰 남았는지 알 수 없지만, 계수 비에 따르면, X는 2/a mol 만큼 생성되고, B2는 b/a mol만큼 소진되어 없어진다. 이를 정리하면 다음과 같다.

이를 정리하면, 0.5a + b = 2 이며, a 와 b는 자연수이어야만 하므로 a = 2, b = 1 외에는 해당하는 조합이 없다. 완성된 반응식은 다음과 같다.

주어진 몰수를 바탕으로 (나)의 반응을 살펴보면, 역시 A2가 모두 반응(한계 반응물)되고, B2가 남는 것을 알 수 있다.

따라서 ㄴ 보기는 참이다.
ㄷ.
A2 3 mol과 B2 1 mol을 반응시킨 결과는 다음과 같다. 따라서 ㄷ 보기는 참이다.
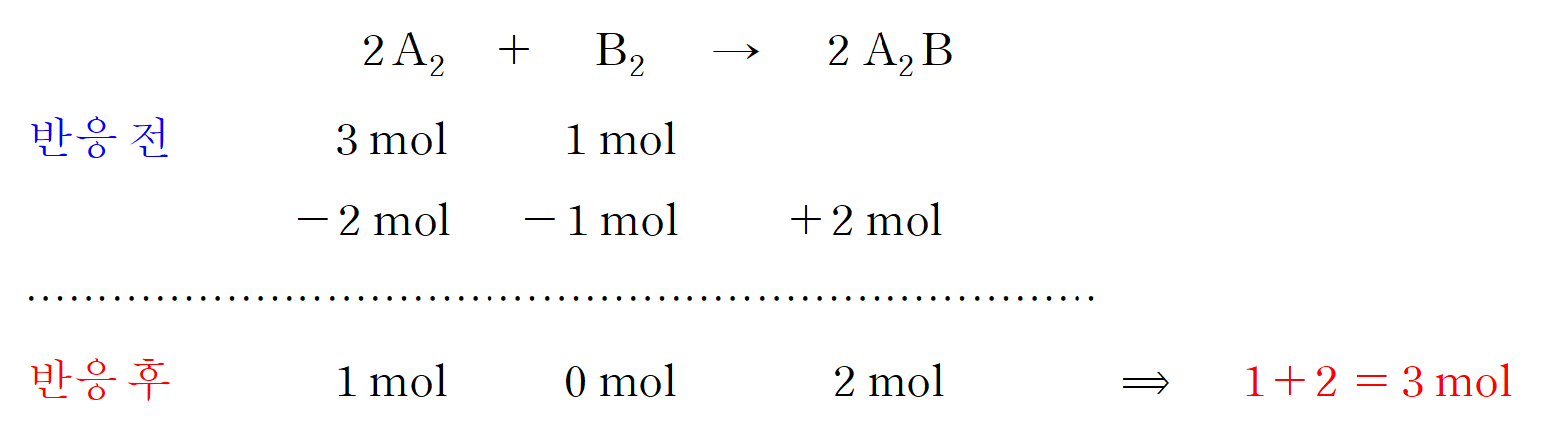
- 끝 -
* 본문 설명 중 잘못된 부분에 대해 지적해주시면 참고하여 수정, 업데이트하도록 하겠습니다. 문제의 출처는 서울시교육청과 EBSi 입니다.
'화학 > 기출풀이' 카테고리의 다른 글
| 2022학년도 10월(10.12.) 고3 전국연합학력평가 화학1 3점 문항 풀이 (0) | 2022.12.15 |
|---|---|
| 2022학년도 10월(10.12.) 고3 전국연합학력평가 화학1 풀이 [20번] (0) | 2022.12.15 |
| 2019학년도 4월(4.10.) 고3 학력평가 화학1 풀이 [10번] (0) | 2021.11.07 |
| 2021학년도 7월(7.7.) 고3 학력평가 화학1 풀이 [19번] (0) | 2021.07.21 |
| 2022학년도 수능 6월 모의평가(2021.6.3.) 화학1 3점 문항 풀이 (0) | 2021.07.19 |



