하메트 식 (The Hammett Equation)
"Quantitative Relationship Between Structure & Reactivity"
하메트 식(Hammett Equation)이란, 하메트(Louis Plack Hammett, 1894-1987)가 콜롬비아 대학 재직 중에 개발한 식으로, 화합물의 구조와 반응성 사이의 관계를 정량적으로 증명한 것이다.
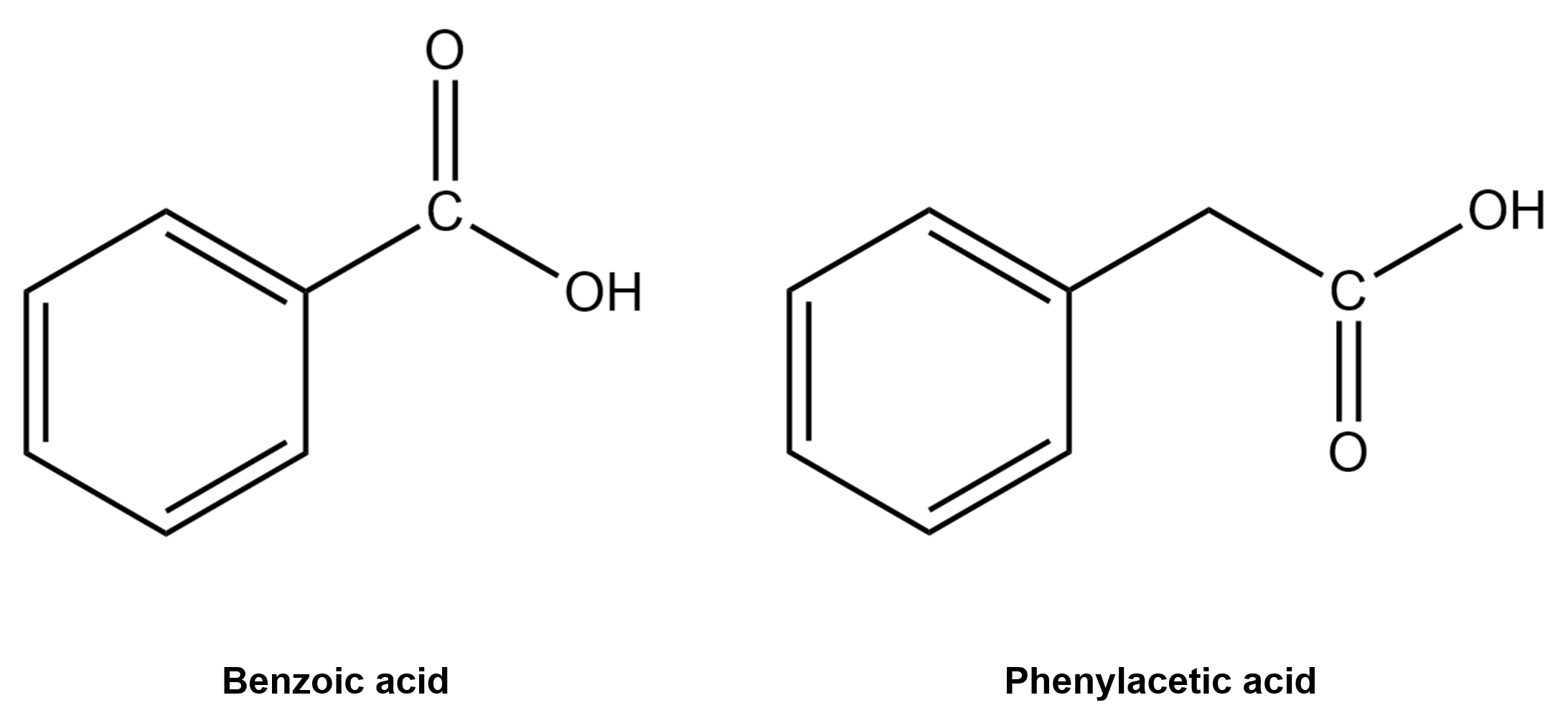
하메트는 벤조산(Benzoic acid)를 기준으로 하고, 치환기 도입 유무에 따른 벤조산의 해리 정도(HA → H+ + A-)를 측정하여 비교하는 방법을 사용했다.

일반적으로 하메트 식은 전자 주개 그룹(EDG, Electron Donating Group)과 전자 끌개 그룹(EWG, Electron Withdrawing Group) 분류의 근거가 되며, 방향족 화합물의 치환기 도입 효과를 정량적으로 확인할 수 있게 하는 지표이다.
하메트 식의 좌변에 위치한 Kz(또는 K 로만 표기하기도 함)는 치환기가 도입된 물질의 산해리 상수이며, K0는 기준 물질(일반적으로 벤조산)의 산해리 상수다. 우변의 rho(ρ)는 반응 상수(reaction constant)로 정의되며, sigma(σ)와 log(Kz/K0)에 대한 그래프에서의 기울기 값이다.
sigma(σ)는 치환기 상수(substituent constant)로, 치환기가 전자를 얼마나 잘 밀어주는가(donating) 또는 잘 끌어당기는가(withdrawing)를 나타내는 척도이다.
1. 치환기 상수(substituent constant, σ)
다양한 치환기 상수(σ) 값을 수집하기 위해서는 기준점이 설정되어야 한다. 측정 물질(Kz)과 기준 물질(K0)이 모두 벤조산이라 한다면, 당연히 Kz = K0이고, 하메트 식의 좌변 log(Kz/K0) 값은 0이 된다. 우변의 반응 상수(ρ)를 1로 기준한다면, 치환기 상수(σ)는 0이다.
이제 측정 대상이 벤조산 아닌, 특정 자리에 치환기 -R 이 도입된 임의 물질이고, 이 물질이 벤조산보다 해리가 잘된다고 가정해보자. 해리가 잘된다는 말은, 해리 반응(HA → H+ + A-)의 평형이 벤조산보다 더 생성물 쪽에 치우쳐있다는 뜻이며, 벤조산보다 큰 평형 상수(Kz > K0) 값을 갖는다는 뜻이다.
좌변의 log 안 값(Kz/K0)은 1보다 크고, 좌변은 0보다 큰 값이 된다. 우변의 반응 상수가 여전히 1일 때, 치환기 상수(σ)는 0보다 큰 양(+)의 값이다.
반대로 치환기를 도입했는데, 벤조산에 비해 덜 해리된다면, 앞선 경우와 반대로 Kz < K0 이고, 치환기 상수(σ)는 0보다 작은 음(-)의 값이 된다.
정리하자면, 치환기가 자신쪽으로 효과적으로 전자를 끌어가(EWG) 산의 해리도를 증가시키면, 치환기 상수(σ) > 0 이고, 반대로 치환기가 전자를 효과적으로 제공하면, 치환기 상수(σ) < 0 이 된다. 따라서 치환기 상수의 부호와 크기에 따라 도입된 치환기가 EWG 또는 EDG로 작용하는지를 구분할 수 있다.
벤조산의 para- 위치에서의 치환기 상수값(σpara)은 다음과 같다.
2. 반응 상수(reaction constant, ρ)
하메트 식의 기울기 상수(ρ)는 임의의 치환기가 도입된 벤조산(x축)의 pKa 값과 벤조산과 구조적 차이를 갖는 화합물(y축)의 pKa 값들을 점찍어 얻어지는 직선의 기울기에 해당한다. 이는 벤조산과의 구조적 차이가 치환기 도입 효과에 어떠한 영향을 주는지를 알 수 있게 해준다.
만약, x축에는 벤조산, y축도 벤조산의 pKa 값으로 그래프를 도시한다면, 당연히 치환기 도입에 의한 결과 또한 같을 것이므로, x값과 y값이 언제나 같은 기울기가 1인 직선 그래프가 그려질 것이다.
그러나 x축에는 벤조산을 기본 구조로 하는 물질들, y축에는 페닐아세트을 기본 구조로 하는 물질들로 달리한 뒤, 메틸기(-CH3), 염소기(-Cl), 나이트로기(-NO2) 등의 치환기를 각각 para-자리에 도입하면서 각 물질들의 산 해리 상수(pKa)를 측정한다. 도입된 치환기 효과에 따라 서로 다른 pKa 값들이 측정될 것이며, 이는 그래프의 x값(벤조산 기본 구조)과 y값(페닐아세트산 기본 구조)이 된다.
측정 결과는 아래 표와 같다. 파라(-para) 자리에 동일한 나이트로기(-NO2)를 도입했음에도 벤조산(x)의 경우 pKa 값이 3.4, 페닐아세트산(y)은 3.9로 차이가 있다. 염소(-Cl)를 치환기로 도입했을 때에도 x = 4.0과 y = 4.2로 다르다.
이러한 방식으로 치환기에 따른 pKa 값을 x, y 좌표로 점찍어 그래프로 나타내면 아래 그래프와 같다.
도시된 그래프의 기울기는 약 0.5이며, 이 값이 페닐아세트산의 반응 상수(ρ)이다. 페닐아세트산의 반응상수가 벤조산의 1보다 작다는 것은 페닐아세트산의 치환기 도입 효과가 벤조산에 비해 덜하다는 뜻이다. 같은 치환기를 같은 자리에 도입해도 해리 반응에 미치는 정도가 크지 않다는 뜻이다.
그 이유를 페닐아세트산의 구조에서 찾아보면, 벤젠 고리와 카복시기(-COOH) 사이에 삽입된 에틸렌기(-CH2)에 의한 거리 증가 요인 때문이라 설명할 수 있겠다. (Question 1)

반응 상수(ρ)의 부호는 어떤 치환기가 반응에 진행에 도움이 되는지를 예측 가능하며, 반응 상수의 크기는 치환기에 얼마나 민감하게 영향을 받는지 알려준다.
양(+)의 반응 상수(기울기)를 갖는다는 것은 전자 끄는기(EWG)가 산의 해리 반응에 도움을 줄 수 있다는 뜻이며, 음(-)의 반응 상수(기울기)를 갖는다는 것은 전자 주는기(EDG)가 오히려 산의 해리 반응에 도움이 된다는 뜻이다.
반응(기울기) 상수의 절댓값이 크다는 것은 산의 구조가 치환기에 영향을 크게 받음을 의미하며, 위에서 제시된 페닐아세트산(ρ=0.489)과 벤조산(ρ=1.0)에서 알 수 있듯이 벤조산이 치환기 도입에 따라 반응의 정도가 더욱 민감하다는 것을 의미한다. 페닐아세트산에 에틸렌기(-CH2)가 하나 더 추가된 경우 반응 상수 값이 0.212까지 감소하는 것을 위의 표에서 확인할 수 있으며, 이는 치환기 도입에 따른 효과가 현저하게 떨어진다는 것을 의미한다.
3. 정리
지금까지의 설명을 바탕으로 앞의 하메트 식을 살펴보면, 화합물의 기본 구조와 도입한 치환기의 종류를 안다면, 해당 화합물의 pKa 값을 예측 가능하다. 예를들어, p-메톡시페닐아세트산(Question 4-c)의 pKa 값을 구해보자. 화합물의 기본 구조가 페닐아세트산이므로 반응 상수(기울기, ρ)는 0.489, 기준이 되는 pKa = - log(K0) = 4.31이다. 도입된 치환기는 메톡시기(-OCH3)이므로 치환기 상수 σ = - 0.27 이다. 각각을 아래의 식에 대입하면, p-메톡시페닐아세트산의 pKa = - logKz 값을 예상할 수 있다.
[참고자료] 2014 1급 정교사 자격연수 - 충북대학교 사범대학 화학교육과 권효식 교수님



* 2022-04-02 구 에디터에서 작성한 글을 현재 양식에 맞게 고치는 과정에서 내용 및 문맥이 일부 수정되었습니다.
'화학 > 화학이야기' 카테고리의 다른 글
| 분자 사이의 힘 (Intermolecular Interaction) (0) | 2017.09.25 |
|---|---|
| 최조밀 쌓음 구조 (closest packing structure) (2) | 2017.09.22 |
| 산과 염기 (acid & base) (0) | 2014.08.18 |
| 이온결합의 공유결합성 (Fajans Rule) (10) | 2014.07.16 |
| 톰슨의 비전하 측정 실험 (2) | 2014.07.13 |








